题目内容
 (1)水是生命的源泉,也是不可缺少的资源.
(1)水是生命的源泉,也是不可缺少的资源.①自来水厂净水过程中需加消毒剂.高铁酸钾(K2FeO4)是一种高效的消毒剂,其中铁元素的化合价为
(2)在其它操作无误情况下,用量筒量取浓硫酸时仰视读数,所配溶液溶质质量分数
考点:有关元素化合价的计算,浓硫酸的性质及浓硫酸的稀释,一定溶质质量分数的溶液的配制,氧气的化学性质,电解水实验
专题:溶液、浊液与溶解度,空气与水
分析:(1)①根据化合物中各元素化合价的代数和为0进行解答;
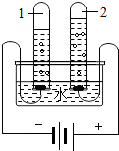
②根据电解水实验过程中氢气和氧气的体积比为2:1进行解答;
③根据铁丝在氧气中燃烧生成四氧化三铁以及注意事项进行解答;
④根据浓硫酸的稀释方法进行分析;
(2)根据溶液稀释过程中溶质不变进行解答.
②根据电解水实验过程中氢气和氧气的体积比为2:1进行解答;
③根据铁丝在氧气中燃烧生成四氧化三铁以及注意事项进行解答;
④根据浓硫酸的稀释方法进行分析;
(2)根据溶液稀释过程中溶质不变进行解答.
解答:解:①由化合物中各元素化合价的代数和为0以及高铁酸钾(K2FeO4)中钾元素的化合价为+1价、氧元素的化合价为-2价,所以铁元素的化合价为+6价;故填:+6;
②电解水实验过程氢气和氧气的体积比为2:1,所以当其中一个电极产生4mL气体时,另一电极产生的气体体积可能是2或8mL;故填:2或8;
③铁丝在氧气中燃烧实验中,集气瓶中盛少量水的目是防止生成物溅落炸裂瓶底;故填:防止生成物溅落炸裂瓶底;
④实验室常用水稀释浓硫酸.操作是一定要将浓硫酸沿着容器壁慢慢注入水中,并不断用玻璃棒搅拌,故填:将浓硫酸沿着容器壁慢慢注入水中;不断用玻璃棒搅拌;
(2)在其它操作无误情况下,用量筒量取浓硫酸时仰视读数,会使得浓硫酸的体积偏大,所配溶液溶质质量分数偏大.故填:偏大.
②电解水实验过程氢气和氧气的体积比为2:1,所以当其中一个电极产生4mL气体时,另一电极产生的气体体积可能是2或8mL;故填:2或8;
③铁丝在氧气中燃烧实验中,集气瓶中盛少量水的目是防止生成物溅落炸裂瓶底;故填:防止生成物溅落炸裂瓶底;
④实验室常用水稀释浓硫酸.操作是一定要将浓硫酸沿着容器壁慢慢注入水中,并不断用玻璃棒搅拌,故填:将浓硫酸沿着容器壁慢慢注入水中;不断用玻璃棒搅拌;
(2)在其它操作无误情况下,用量筒量取浓硫酸时仰视读数,会使得浓硫酸的体积偏大,所配溶液溶质质量分数偏大.故填:偏大.
点评:本题为涉及较多的化学基础知识,题目难点不大但涉及面较广,耐心审题、沉着作答对于解答类似问题会有较大帮助.

练习册系列答案
相关题目
X、Y、Z、W、Q均为含氮的化合物,在一定条件下,将发生如下转换关系(未配平)
①X→W+O2
②Z+Y+NaOH→H2O+W
③Y+SO2→Z+SO3
④Q+Y→Z+H2O
⑤X+Cu+H2SO4→Cu2++Y+SO42-
这五种化合物中氮元素的化合价由高到低的顺序为( )
①X→W+O2
②Z+Y+NaOH→H2O+W
③Y+SO2→Z+SO3
④Q+Y→Z+H2O
⑤X+Cu+H2SO4→Cu2++Y+SO42-
这五种化合物中氮元素的化合价由高到低的顺序为( )
| A、XYZWQ |
| B、XZYQW |
| C、XYWZQ |
| D、WXZQY |
下列物质的化学式书写正确的是( )
| A、氧化锌--ZnO2 |
| B、氯化氢--ClH |
| C、氢氧化钾--KOH |
| D、硫酸铝--AlSO4 |
下列物质的用途中,与其化学性质有关的是( )
| A、坚硬的金刚石用于切割玻璃 |
| B、镁粉用于照明弹 |
| C、氢气用于充灌气球 |
| D、活性炭做吸附剂 |
工业生产或生活中常见的下列现象所发生的变化中,属于物理变化的是( )
| A、食物腐败 | B、水结成冰 |
| C、用铁矿石炼铁 | D、蜡烛燃烧 |
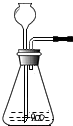 如图在制取气体的实验中,所添加的液体药品的量要
如图在制取气体的实验中,所添加的液体药品的量要 如图所示:
如图所示: 如图是浓盐酸试剂瓶标签的部分内容.请回答:
如图是浓盐酸试剂瓶标签的部分内容.请回答: