题目内容
【题目】某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取12.5g样品加入到稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示,请回答: 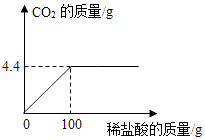
(1)该实验最多制得CO2的质量为g.
(2)该碳酸钙样品的纯度为 .
(3)计算所加稀盐酸的溶质质量分数.(要求有计算过程)
【答案】
(1)4.4
(2)80%
(3)解:由图可以看出生成的二氧化碳的质量为4.4g.
设参加反应的碳酸钙的质量为x,HCl的质量为y.
CaCO3+ | 2HCl=CaCl2+H2O+ | CO2↑ |
100 | 73 | 44 |
x | y | 4.4g |
![]() =
= ![]() =
= ![]()
x=10g
y=7.3g
则样品中碳酸钙的质量分数即纯度为 ![]() ×100%=80%
×100%=80%
所用盐酸中溶质的质量分数 ![]() ×100%=7.3%.
×100%=7.3%.
【解析】解:由图可以看出生成的二氧化碳的质量为4.4g. 设参加反应的碳酸钙的质量为x,HCl的质量为y.
CaCO3+ | 2HCl=CaCl2+H2O+ | CO2↑ |
100 | 73 | 44 |
x | y | 4.4g |
![]()
x=10g
y=7.3g
则样品中碳酸钙的质量分数即纯度为 ![]() ×100%=80%
×100%=80%
所用盐酸中溶质的质量分数 ![]() ×100%=7.3%.
×100%=7.3%.
答案为:(1)4.4; (2)80%;(3)7.3%.
【考点精析】关于本题考查的根据化学反应方程式的计算,需要了解各物质间质量比=系数×相对分子质量之比才能得出正确答案.

练习册系列答案
相关题目
【题目】某地农业科技工作者在进行“酸雨对农业产量影响及对策的研究”中,得出酸雨的pH大小与小麦减产幅度关系的一组数据如下表所示。根据数据判断,下列说法正确的是( )
酸雨pH | 3.58 | 4.59 | 4.86 |
小麦减产(%) | 10 | 5 | 3 |
A.酸雨的pH越大,小麦减产幅度越大
B.酸雨的pH越小,小麦减产幅度越大
C.酸雨的酸性越强,小麦的减产越小
D.酸雨的酸性越强,小麦的减产越大