题目内容
【题目】化学课外兴趣小组的同学取用一定质量的石灰石样品,把50.0 g稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
实验次数 | 1 | 2 | 3 | 4 | 5 |
稀盐酸的加入量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体的质量/g | 3.0 | 2.0 | 1.0 | m | 0.6 |
则下列有关说法不正确的是( )
A.石灰石样品的质量为4 gB.m的值为0.8 g
C.石灰石中碳酸钙的质量分数为85%D.稀盐酸中溶质质量分数为7.3%
【答案】B
【解析】
A、由一、二、三次实验可知,每次反应的碳酸钙的质量是1g,因此石灰石样品的质量为4g,该选项说法正确;
B、第三次剩余固体的质量是1.0g,因为含有杂质,因此碳酸钙的质量不足1.0g,第四次加入10g稀盐酸后,碳酸钙应该完全反应,剩余固体的质量应该和第五次剩余固体的质量相等,因此m的值为0.6g,该选项说法不正确;
C、石灰石中碳酸钙的质量分数为:![]() ×100%=85%,该选项说法正确;
×100%=85%,该选项说法正确;
D、设10g稀盐酸中氯化氢的质量为x,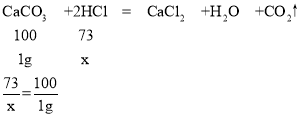
x=0.73g,
稀盐酸中溶质质量分数为:![]() ×100%=7.3%,该选项说法正确。
×100%=7.3%,该选项说法正确。
故选:B。

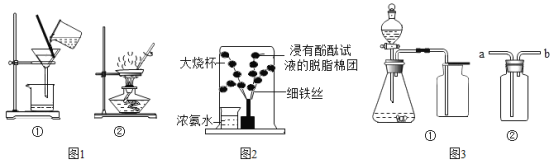
【题目】在学习酸的化学性质后,同学们做了如下两个实验:
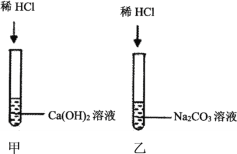
(观察与讨论1)实验时,甲试管中没有观察到明显现象,同学们对氢氧化钙和盐酸是否发生化学反应表示怀疑。请你写出能观察到该化学反应发生的一种方法_______________。
(观察与讨论2)实验结束后,同学们将两支试管中的物质倒入同一洁净的烧杯中,观察到烧杯中先有气泡产生,然后出现白色沉淀。经过讨论确定,甲试管中废液含有的溶质是________________(填化学式,下同),乙试管中废液含有的溶质是________________。为科学处理实验后产生的废液,同学们决定对烧杯中最终废液溶质的成分进行探究。
(提出问题)最终废液中溶质成分是什么?
(猜想与假设)猜想1:NaCl。
猜想2:NaCl、CaCl2。
猜想3:________________。
(实验探究)请你设计实验证明猜想3是正确的,并完成下列实验报告。
实验步骤 | 实验现象 | 实验结论 |
__________________ | __________________ | 猜想3正确 |
(反思交流)随着大家环保意识的增强,实验室产生的污染越来越受到重视,实验中产生的污染物必须无害化处理后再排放。
【题目】为了测定某碳酸钠样品中杂质氯化钠的质量分数,李明同学进行了三次实验,实验数据如下表:完成下列计算:
编 号 | 第1次 | 第2次 | 第3次 |
所取固体样品的质量/g | 7 | 5 | 5 |
加入氯化钙溶液的质量/g | 50 | 50 | 75 |
反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)碳酸钠样品中碳酸钠的质量是多少______________?(如不整除计算结果精确到0.1%,下同)
(2)加入氯化钙溶液的溶质质量分数是多少______________?
(3)恰好反应时所得溶液的溶质质量分数______________?