��Ŀ����
����Ŀ��Ϊ�˲ⶨij̼������Ʒ�������Ȼ��Ƶ���������������ͬѧ����������ʵ�飬ʵ���������±���������м��㣺
�� �� | ��1�� | ��2�� | ��3�� |
��ȡ������Ʒ������/g | 7 | 5 | 5 |
�����Ȼ�����Һ������/g | 50 | 50 | 75 |
��Ӧ�����ɳ���������/g | 4 | 4 | 4 |
��1��̼������Ʒ��̼���Ƶ������Ƕ���______________�����粻������������ȷ��0.1������ͬ��
��2�������Ȼ�����Һ���������������Ƕ���______________��
��3��ǡ�÷�Ӧʱ������Һ��������������______________��
���𰸡�4.24g 8.9% 10.7%
��������
��1�����������������ʵ�����ݿ�֪����һ�κ͵ڶ�����ȡ�Ĺ����������ȣ�������ȡ�Ȼ�����Һ��������ȣ����ɵij�����������ȣ����Կ����жϵ�һ����ȡ������ʣ�࣬��5g����Ʒ��Ӧ�������ɳ���������Ϊ4g����2�κ͵�3����ȡ�Ĺ�����Ʒ��ȣ�������ȡ���Ȼ�����Һ���������ȣ����ɵij�����������ȣ����Կ����жϵ�3����ȡ���Ȼ�����Һ��ʣ�࣬��˵��50g�Ȼ�����Һ��Ӧ��ֻ�ܵõ�4g���������Ϸ�������֪���ڶ���������������ǡ����ȫ��Ӧ��
��̼���Ƶ�����Ϊx���μӷ�Ӧ���Ȼ�������Ϊy�������Ȼ��Ƶ�����Ϊz��
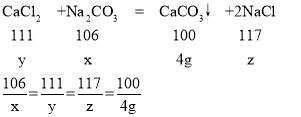
��ã�x=4.24g��y=4.44 g z=4.68g
��2��������Ȼ�����Һ��������������Ϊ��![]() ��100%��8.9%��
��100%��8.9%��
��3��ǡ�÷�Ӧʱ������Һ���������������ǣ�![]() ��100%=10.7%��
��100%=10.7%��
�𣺣�1��̼������Ʒ��̼���Ƶ�������4.24g��
��2�������Ȼ�����Һ����������������8.9%��
��3��ǡ�÷�Ӧʱ������Һ��������������10.7%��

����Ŀ����ѧ������ȤС���ͬѧȡ��һ��������ʯ��ʯ��Ʒ����50.0 gϡ�������μ�����Ʒ�У���Ʒ�е����ʼȲ������ᷴӦ��Ҳ������ˮ����ÿ�γ�ַ�Ӧ�����ˡ������������ʵ���������£�
ʵ����� | 1 | 2 | 3 | 4 | 5 |
ϡ����ļ�����/g | 10 | 10 | 10 | 10 | 10 |
ʣ����������/g | 3.0 | 2.0 | 1.0 | m | 0.6 |
�������й�˵������ȷ���ǣ� ��
A.ʯ��ʯ��Ʒ������Ϊ4 gB.m��ֵΪ0.8 g
C.ʯ��ʯ��̼��Ƶ���������Ϊ85%D.ϡ������������������Ϊ7.3%