题目内容
【题目】小美同学在取用生石灰干燥剂时,发现装满生石灰的塑料瓶已经膨胀破裂。下面是兴趣小组对生石灰是否变质的探究实验,请你参与到其中去,回答下列有关问题:
(1)生石灰干燥剂能吸水的原因是________________(用化学方程式表示)。
(提出问题)该瓶干燥剂的成分是什么?
(做出猜想)猜想1:含有CaO;
猜想2:含有Ca(OH)2 ;
猜想3:含有CaCO3。
(进行实验)
实验步骤 | 实验现象 | 结论 |
I.取少量干燥剂于试管中,向试管中加入少量的水,用手触摸试管外壁 | 试管外壁有热感 | 含有_______ |
Ⅱ.向步骤I加水后的试管中滴入无色酚酞溶液 | 溶液变红色 | 含有Ca(OH)2 |
Ⅲ.向进行完步骤II 的试管中加入足量的稀盐酸 | _______ | 含有CaCO3 |
(实验分析)小明同学认为步骤Ⅱ不能确定Ca(OH)2是否存在,原因是________________。
(改进实验)小明同学取该瓶干燥剂进行如下实验;
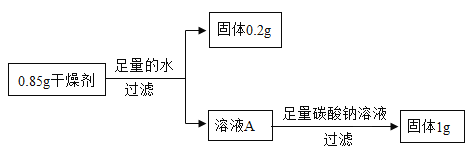
(2)根据小明的实验结果,干燥剂中含有的物质是________________。
(拓展延伸)通过上述探究实验,同学们向实验室提出保存、使用易变质的试剂时的建议,其中合理的是___(填字母)。
A 密封保存 B 使用完后及时盖好瓶盖 C 禁止使用这种试剂
【答案】![]() CaO 有 气泡产生 氧化钙与水反应也会生成氢氧化钙 CaO、Ca(OH)2、CaCO3 AB
CaO 有 气泡产生 氧化钙与水反应也会生成氢氧化钙 CaO、Ca(OH)2、CaCO3 AB
【解析】
(1)生石灰能够吸水的原因是氧化钙与水反应生成氢氧化钙,反应的方程式为:![]() ;
;
[进行实验]Ⅰ、取少量干燥剂于试管中,向试管中加入少量的水,用手触摸试管外壁,试管外壁有热感,是因为氧化钙溶于水放热,说明固体中含有氧化钙;Ⅲ.向进行完步骤Ⅱ的试管中加入足量的稀盐酸,溶液由红色变成无色,产生气泡,是因为盐酸先和氢氧化钙反应生成氯化钙和水,后和碳酸钙反应生成氯化钙、水和二氧化碳,说明固体中含有碳酸钙。
故填:CaO;产生气泡。
[实验分析] 小明同学认为步骤Ⅱ不能确定Ca(OH)2是否存在,原因是氧化钙能和水反应生成氢氧化钙。
故填:氧化钙能和水反应生成氢氧化钙。
(2)0.2g固体是碳酸钙,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式及其质量关系:
CaO+H2O=Ca(OH)2,Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,可以得到:,

由以上质量关系可知,生成1g碳酸钙时,需要氧化钙的质量是0.56g,而除去碳酸钙外固体质量是:0.85g-0.2g=0.83g,说明固体中含有氢氧化钙,因此固体中同时含有氧化钙、氢氧化钙和碳酸钙。
故填:氧化钙、氢氧化钙和碳酸钙。
【拓展延伸】
(1)通过上述探究实验,同学们向实验室提出保存、使用易变质的试剂时的建议,其中合理的是密封保存,使用完后及时盖好瓶盖。
故选:AB。

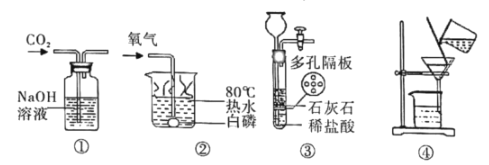
【题目】结合下列装置回答问题。
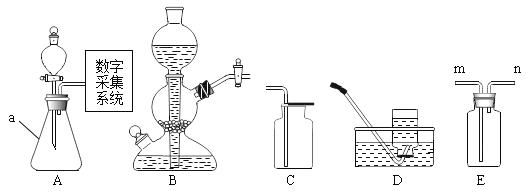
①仪器a的名称是_________________。
②装置B中的活塞处于______ (选填“开启”或“关闭”)状态。
③实验室制取二氧化碳的化学方程式为______, 若用装置E收集二氧化碳,验满时燃着的木条应放在______(选填“m”或“n”)端。
④化学兴趣社团借助数学化实验手段用装置A探究“外界条件对过氧化氢分解速率的影响”,按下表分组进行实验一, 在同一温度下通过压强传感器得到的数据如下图所示。

实验一 | 药品 |
第一组 | 4%H2O2溶液15mL |
第二组 | 4%H2O2溶液15mL、0.2gMnO2粉末 |
第三组 | 4%H2O2溶液15mL、0.2gFeCl3粉末 |
I .经过分组实验,同学们从实验一中得出结论: 在其他条件相同的情况下,____ (填物质名称)作催化剂的催化效果最好。
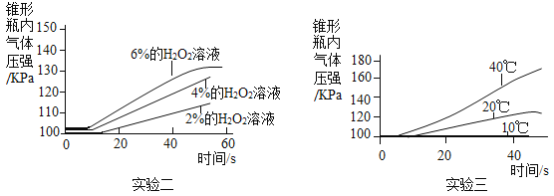
II .选用0.2g的MnO2粉末做催化剂,同学们又分别做了实验二和实验三,得到的数据图表如上,你认为影响该反应速率的外界因素除催化剂外,还有_________。
Ⅲ.实验一与实验二中4%的过氧化氢溶液与0.2g MnO2粉末混合后产生的气体压强有明显不同(见图中A点和B点),你认为可能的原因是_________。
⑤小组同学若利用过氧化氢制取0.1mol氧气,需要过氧化氢的物质的量为多少_____?(根据化学方程式计算)