题目内容
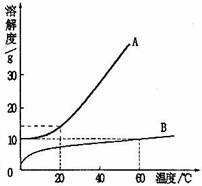
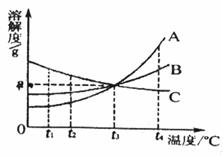
 固体A、B的溶解度曲线如图所示.
固体A、B的溶解度曲线如图所示.(1)10℃时,50g水中分别溶解A、B达饱和,溶解的较少的物质是
B
B
.(2)30℃时,把70g B物质加入100g水中,然后从30℃降温到20℃,此时B溶液的质量分数是
28.6%
28.6%
.(3)B的溶液中混有少量的A,要从溶液中得到B的晶体,宜采用的方法是
冷却热饱和溶液
冷却热饱和溶液
.分析:(1)根据10℃时A、B的溶解度分析判断;
(2)根据B在30℃、20℃的溶解度及溶质的质量分数计算式分析解答;
(3)B的溶解度随温度变化大,A的溶解度随温度的升高变化较小.
(2)根据B在30℃、20℃的溶解度及溶质的质量分数计算式分析解答;
(3)B的溶解度随温度变化大,A的溶解度随温度的升高变化较小.
解答:解:(1)10℃时A的溶解度大于B的溶解度,所以10℃时,50g水中分别溶解A、B达饱和,溶解的B较少;
故答案为:B;
(2)B在30℃时的溶解度是60g,故30℃时,把70g B物质加入100g水中形成的是饱和溶液;20℃时B的溶解度是40g,即100g水中最多溶解40g的B,故其溶质的质量分数是
×100%=28.6%;
故答案为:28.6%;
(3)B的溶解度随温度变化大,A的溶解度随温度的升高变化较小;所以B的溶液中混有少量的A,要从溶液中得到B的晶体,宜采用的方法是冷却热饱和溶液;
故答案为:冷却热饱和溶液.
故答案为:B;
(2)B在30℃时的溶解度是60g,故30℃时,把70g B物质加入100g水中形成的是饱和溶液;20℃时B的溶解度是40g,即100g水中最多溶解40g的B,故其溶质的质量分数是
| 40g |
| 140g |
故答案为:28.6%;
(3)B的溶解度随温度变化大,A的溶解度随温度的升高变化较小;所以B的溶液中混有少量的A,要从溶液中得到B的晶体,宜采用的方法是冷却热饱和溶液;
故答案为:冷却热饱和溶液.
点评:本题着重考查了对溶解度概念的理解,以及溶解度曲线的应用、溶质质量分数的计算,难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
下表是硫酸亚铁晶体在相应温度时的溶解度数据,以及在对应条件下溶液中析出固体的化学式.
| 曲 线 | A | B | |||||||
| 温度[t(℃)] | 0 | 10 | 20 | 30 | 40 | 50 | 70 | 80 | 90 |
| 溶解度[S(g)] | 15.65 | 20.51 | 26.5 | 32.9 | 40.2 | 48.6 | 50.9 | 43.6 | 37.3 |
| 溶液中析出 固体的化学式 | FeSO4?7H2O | FeSO4?H2O | |||||||
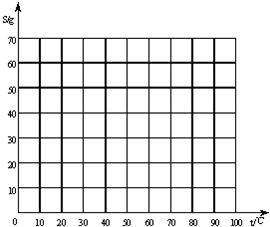
(2)在交点P处所代表的溶液中,溶质质量分数为______(填:“最小”或“最大”)
(3)请在箭号的上、下处填写合理的温度数据,以表示下列关系式的成立.[其中,化学式后括号内的字母含义:“S”代表固体;“L”代表液体.]
FeSO4?7H2O(S)
 FeSO4?H2O(S)+6H2O(L)
FeSO4?H2O(S)+6H2O(L)
下表是硫酸亚铁晶体在相应温度时的溶解度数据,以及在对应条件下溶液中析出固体的化学式.
(1)请你利用上表中相关数据,在坐标格内绘制A和B两条溶解度曲线,并根据曲线A、B的趋势,将A向右、B向左自然延伸直至两条曲线相交为止,得到交点P.
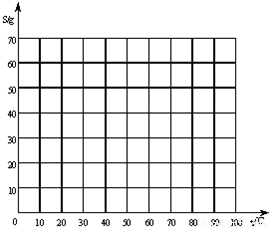
(2)在交点P处所代表的溶液中,溶质质量分数为______(填:“最小”或“最大”)
(3)请在箭号的上、下处填写合理的温度数据,以表示下列关系式的成立.[其中,化学式后括号内的字母含义:“S”代表固体;“L”代表液体.]
FeSO4?7H2O(S) FeSO4?H2O(S)+6H2O(L)
FeSO4?H2O(S)+6H2O(L)
| 曲 线 | A | B | |||||||
| 温度[t(℃)] | 10 | 20 | 30 | 40 | 50 | 70 | 80 | 90 | |
| 溶解度[S(g)] | 15.65 | 20.51 | 26.5 | 32.9 | 40.2 | 48.6 | 50.9 | 43.6 | 37.3 |
| 溶液中析出 固体的化学式 | FeSO4?7H2O | FeSO4?H2O | |||||||

(2)在交点P处所代表的溶液中,溶质质量分数为______(填:“最小”或“最大”)
(3)请在箭号的上、下处填写合理的温度数据,以表示下列关系式的成立.[其中,化学式后括号内的字母含义:“S”代表固体;“L”代表液体.]
FeSO4?7H2O(S)
 FeSO4?H2O(S)+6H2O(L)
FeSO4?H2O(S)+6H2O(L)
 FeSO4?H2O(S)+6H2O(L)
FeSO4?H2O(S)+6H2O(L)