题目内容
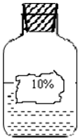 29、小明在化学实验室发现一瓶无色溶液如图,老师告诉他,这瓶可能是氢氧化钠、氯化钠、碳酸钠、浓硫酸四种溶液中的一种(实验时可用的药品有:KNO3、BaCl2、稀盐酸三种溶液).
29、小明在化学实验室发现一瓶无色溶液如图,老师告诉他,这瓶可能是氢氧化钠、氯化钠、碳酸钠、浓硫酸四种溶液中的一种(实验时可用的药品有:KNO3、BaCl2、稀盐酸三种溶液).(1)小明根据信息立即确定该溶液不可能是浓硫酸,理由是
浓硫酸的溶质质量分数不可能是10%
.(2)小明取样品,滴加无色酚酞试液,试液变红色,小明判断该溶液可能是
氢氧化钠溶液
_或碳酸钠溶液
.为了进一步验证该溶液,小明又取样品,加入适量的稀盐酸
,现象若有气泡产生(或无现象)
,该溶液是碳酸钠溶液(或氢氧化钠溶液)
.分析:(1)根据常浓硫酸的质量分数排除是浓硫酸的可能性;
(2)根据溶液能使无色酚酞试液变红显碱性可排除是氯化钠的可能;由于氢氢化钠和碳酸钠都显碱性,可根据二者的组成情况选择方法进行鉴别.
(2)根据溶液能使无色酚酞试液变红显碱性可排除是氯化钠的可能;由于氢氢化钠和碳酸钠都显碱性,可根据二者的组成情况选择方法进行鉴别.
解答:解:(1)浓硫酸的溶质质量分数不可能是10%,而该无色溶液溶质的质量分数为10%,所以不可能为浓硫酸;
(2)该溶液中加入无色酚酞试液会变成红色,可知溶液显碱性,剩下的氢氧化钠、氯化钠、碳酸钠溶液三种溶液中氢氧化钠、碳酸钠溶液显碱性而氯化钠显中性,故可能是氢氧化钠和碳酸钠;氢氧化钠、碳酸钠溶液中,因碳酸钠溶液中含有碳酸根离子加入稀盐酸应该会有气体产生,而氢氧化钠与稀盐酸反应生成可溶于水的氯化钠和水没有明显的实验现象,可以取样品加入适量稀盐酸,若有气泡产生,该溶液是碳酸钠溶液,若无现象,则该溶液为氢氧化钠溶液.
故答案为:
(1)浓硫酸的溶质质量分数不可能是10%;
(2)氢氧化钠溶液、碳酸钠溶液;稀盐酸,若有气泡产生(或无现象),碳酸钠溶液或氢氧化钠溶液.
(2)该溶液中加入无色酚酞试液会变成红色,可知溶液显碱性,剩下的氢氧化钠、氯化钠、碳酸钠溶液三种溶液中氢氧化钠、碳酸钠溶液显碱性而氯化钠显中性,故可能是氢氧化钠和碳酸钠;氢氧化钠、碳酸钠溶液中,因碳酸钠溶液中含有碳酸根离子加入稀盐酸应该会有气体产生,而氢氧化钠与稀盐酸反应生成可溶于水的氯化钠和水没有明显的实验现象,可以取样品加入适量稀盐酸,若有气泡产生,该溶液是碳酸钠溶液,若无现象,则该溶液为氢氧化钠溶液.
故答案为:
(1)浓硫酸的溶质质量分数不可能是10%;
(2)氢氧化钠溶液、碳酸钠溶液;稀盐酸,若有气泡产生(或无现象),碳酸钠溶液或氢氧化钠溶液.
点评:本题根据氢氧化钠、氯化钠、碳酸钠和浓硫酸几种物质的性质特点,采取“先排除,最后进行实验检验的”方法确定未知溶液.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目