题目内容
【题目】某化合物R在空气中完全燃烧,消耗氧气9.6g,生成二氧化碳8.8g、水5.4g,则化合物R中含有种元素.
【答案】三
【解析】解:因为产物中有氢、碳元素组成,所以化合物中一定含有氢、碳元素;
设某化合物为X.则有
X+O2 |
| CO2+ | H2O |
9.6g | 8.8g | 5.4g |
生成物CO2中氧元素质量为:8.8g× ![]() =6.4g
=6.4g
生成物H2O中氧元素质量为:5.4g× ![]() =4.8g
=4.8g
生成物中氧元素质量为:6.4g+4.8g=11.2g.超过反应物的氧气的9.6g,故此X物质也含氧元素.
所以答案是:三
【考点精析】解答此题的关键在于理解质量守恒定律及其应用的相关知识,掌握①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏.

 科学实验活动册系列答案
科学实验活动册系列答案【题目】某石灰石厂实验室用5.55g石灰石样品高温煅烧制得生石灰和二氧化碳分析,该实验室进行了四次高温中加热,并冷却后称量,记录数据如表(杂质不参加反应).
操作次数 | 1 | 2 | 3 | 4 |
剩余固体质量(g) | 4.25 | 3.95 | 3.35 | 3.35 |
计算:
(1)完全反应后生成二氧化碳的质量.
(2)求石灰石中碳酸钙的质量分数是多少?
(3)求分析产品中生石灰的质量分数是多少?
【题目】碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
(1)实验一:探究碳酸氢钠溶液的酸碱性
取碳酸氢钠溶液少许,滴加无色酚酞溶液变红,由此可知碳酸氢钠溶液呈性.
(2)实验二:探究碳酸氢钠的热稳定性
[查阅资料]碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
[进行实验]为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示.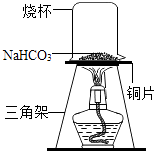
Ⅰ、加热一段时间后,观察到烧杯内壁有生成.
Ⅱ、充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式: .
Ⅲ、兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3 .
①兴趣小组的同学猜想的依据是 .
②请设计实验检验反应后的固体产物是NaOH还Na2CO3 , 并填入表中:
实 验 操 作 | 预期实验现象 | 结 论 |
取少量固体产物,向其中加入 . | 有气泡产生 | 固体产物是Na2CO3 , 而不是NaOH. |