题目内容
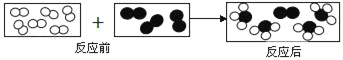
【题目】早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
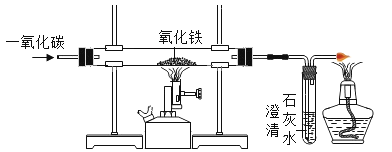
(1)除CO外,还有哪些物质可以还原Fe2O3?_____(请写一种物质的化学式)。
(2)实验中盛澄清石灰水的试管中可观察到的现象是_____。
(3)右边导气管口放置点燃的酒精灯的目的是_____。
(4)实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是_____。
(5)钢是通过生铁炼制成的,在炼钢的过程中用纯氧而不用空气的原因是_____。
【答案】C(或H2) 石灰水变浑浊 燃烧多余的CO(或消除CO对空气的污染) 在右端导气管口用排水法收集一试管气体,移近火焰,若发出轻微的爆鸣声,证明空气已经排尽 促使反应更加剧烈,并获得更多的热量
【解析】
(1)除CO外,具有还原性的物质还有C(或H2)等,也可以还原Fe2O3;
(2)在高温条件下,一氧化碳与氧化铁反应,生成的二氧化碳能使澄清的石灰水变浑浊;
(3)由于尾气中含有一氧化碳,能污染空气;所以,右边导气管口放置点燃的酒精灯的目的是燃烧多余的CO;
(4)如果装置中的空气已排尽,装置内就是纯净的一氧化碳,检验的方法是:在右端导气管口用排水法收集一试管气体,移近火焰,若发出轻微的爆鸣声,证明空气已经排尽;
(5)炼钢是进一步除去炼出的铁中的杂质的过程,利用的是氧气与杂质金属反应;因为杂质含量本来就不多,所以如果采用空气的话,氧气含量只有不到五分之一,与杂质金属接触的几率更小了,不利于除杂,空气中还含有一部分杂质气体很难从钢水中除去;同时由于氧气与杂质反应剧烈放热,为反应进行提供了热量,便于达到熔点,提高钢材坚韧度等指标。综合以上论述,在炼钢的过程中用纯氧而不用空气的原因是:促使反应更加剧烈,并获得更多的热量。

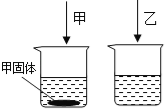
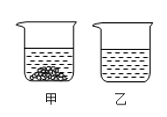
【题目】氯化钠(NaCl) 和硝酸钾 (KNO3) 在不同温度时的溶解度如下表,20℃时甲乙两个烧杯中各有100g水,分别都加入质量为m的氯化钠和硝酸钾固体,充分溶解后如图所示:
温度(℃) | 10 | 20 | 40 | 60 | 80 | |
溶解 度/g | KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 | |
(1)氯化钠和硝酸钾两种物质中,溶解度受温度影响较大的是_____________。
(2)甲中溶解的物质是__________。
(3)常温下配制100g氯化钠的饱和溶液,所需的玻璃仪器有___________。
(4)下列说法正确的是___________
A 若将甲、乙烧杯中的溶液都升温到40℃,所得溶液均不饱和
B 若将甲、乙烧杯中的溶液都降温到10℃,可能都会有固体析出
C 若向甲中加入20g水,则甲中的溶液一定变为不饱和
D 硝酸钾中混有少量的氯化钠,可采用蒸发结晶的方法提纯硝酸钾