题目内容
【题目】化学课外活动小组的某位同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下:

请回答下列问题:
(1)该同学制得氧气的质量为________g。
(2)计算滤液中溶质质量分数。(忽略水的损耗,写出计算过程)
(3)在图中画出氯酸钾分解生成KCl和O2的质量关系图。并在坐标轴上标出一组对应数据。
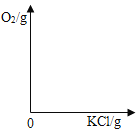
【答案】(1) 4.8 (2) 14.9% (详见解析) (3) 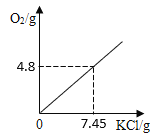
【解析】
氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,根据反应的化学方程式及其提供数据可以进行相关方面的计算。
(1)据质量守恒定律可知,氧气的质量为16.5g-11.7g=4.8g
(2)设生成KCl的质量为x

![]()
x=7.45g
所得滤液的溶质质量分数: ![]() ×100%=14.9%
×100%=14.9%
答:所得KCl溶液的溶质质量分数14.9%。
(3)根据上述计算可知,生成7.45g的氯化钾,同时生成4.8g的氧气,图像的起点为零,氧气的质量与氯化钾质量正比。图像如图(数据标7.45和4.8的倍数时也得分,2分)


练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
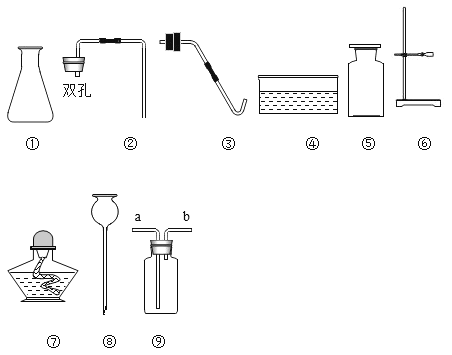
【题目】化学是以实验为基础的学科,根据实验一、二、三回答下列问题。
实验一 | 实验二 | 实验三 |
|
|
|
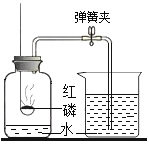
(1)实验一:待红磷熄灭冷却后,打开弹簧夹,观察到集气瓶内水面上升_____,该现象说明氮气的化学性质稳定。
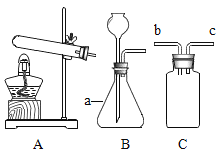
(2)实验二:实验室制取O2和CO2能共用的发生装置是_____,仪器a的名称是_____。若用C装置收集二氧化碳气体,请把导管图补充完整,并在b、c处标明气体流动的方向_____。
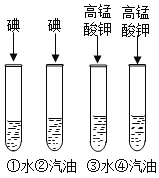
(3)实验三:将试管②和④的现象相比较得到的结论是_____。