题目内容
【题目】(4分)下图是甲、乙两种物质的溶解度曲线,看图回答下列问题:
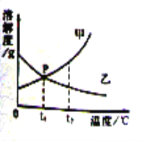
(1)P点的含义是 。
(2)青海盐湖地区有一种说法,“冬天捞碱,夏天晒盐”。其中“碱”的溶解度曲线与图中 (填“甲”或“乙”)物质的溶解度曲线相似。
(3)欲使接近饱和的甲溶液变成饱和溶液,可以采取的方法是 (答一种即可)。
(4)等质量的甲、乙二种物质的饱和溶液从t2℃降温到t1℃时,甲溶液的质量 (填“>”、“<”或“=”)乙溶液的质量。
【答案】(1)t1℃时,甲乙两种物质的溶解度相等 (2)甲
(3)加溶质(蒸发溶剂、降温) (4)<
【解析】
试题分析:(1)根据溶解度曲线,P点的含义是:t1℃时,甲乙两种物质的溶解度相等
(2)“冬天捞碱,夏天晒盐”,说明碱的溶解度随温度的升高变化较大,而盐的溶解度随温度的升高而变化不大,其中“碱”的溶解度曲线与图中甲物质的溶解度曲线相似
(3)根据溶解度曲线,甲的溶解度随温度的升高而增大,故欲使接近饱和的甲溶液变成饱和溶液,可以采取的方法是加溶质(蒸发溶剂、降温)
(4)根据溶解度曲线,甲的溶解度随温度的升高的变化趋势比乙要更大,故将等质量的甲、乙二种物质的饱和溶液从t2℃降温到t1℃时,甲析出的晶体量更大,故甲溶液的质量 <乙溶液的质量

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案【题目】(9分)某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应)。草酸晶体(H2C2O4·2H2O)的部分理化性质见下表:
熔 点 | 沸 点 | 热 稳 定 性 | 与 碱 反 应 |
101℃~102℃ | 150℃~160℃ 升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |
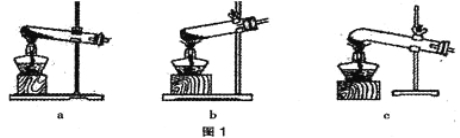
(1)图1是加热装置。最适宜的加热分解草酸晶体装置是 。
(2)图 2 是验证热分解产物中含 CO 、CO2的装置。
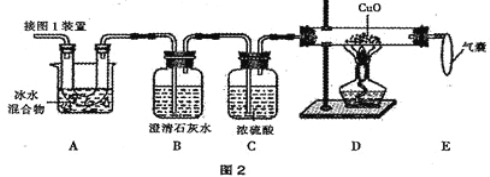
①装置 A 的主要作用是_______________ _ _____。
②气囊的作用是____________________。
③证明存在 CO2的现象是_ ,B中反应的化学方程式 。
④证明存在 CO 的现象是_______ _______。
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因_______(写一条即可)。
(4)称取17.5g草酸晶体样品配制50.00g溶液,加适量的稀硫酸,然后滴加KMnO4 溶液(含KMnO47.9克) 恰好反应完全。
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)
请计算样品中草酸晶体(H2C2O4·2H2O )的质量分数。(写出计算过程)
[有关物质的相对分子质量:Mr(H2C2O4)=90,Mr(H2C2O42H2O)=126,Mr(KMnO4)=158 ]