题目内容
有13.5克CuCl2样品,与足量硝酸银反应得29克氯化银,问在氯化钙、氯化锌、氯化钾、氯化钡中,氯化铜掺了哪一种杂质?
考点:根据化学反应方程式的计算
专题:推断混合物的可能组成
分析:先假设13.5g全部是氯化铜,根据化学方程式计算出生成沉淀的质量,如果实际生成的沉淀质量>假设13.5g全部是氯化铜时生成的沉淀质量,则说明杂质物质中氯元素的质量分数要大于氯化铜中氯元素的质量分数.
解答:解:假设13.5g全部是氯化铜,设生成沉淀的质量为x,
CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2
135 287
13.5g x
=
x=28.7g.
由计算可知,实际生成的沉淀29g>假设13.5g全部是氯化铜时生成的沉淀28.7g.
如果多生成沉淀的话,则应该样品中的Cl的离子数应该是比纯的CuCl2含有的Cl离子数多,相同质量的物质中含有的离子多的话,应该是杂质中含氯离子的那个物质的相对分子质量应该比铜小.因此可以这么说杂质中的氯元素的质量分数比CuCl2中氯元素的质量分数大.氯化铜中铜、氯元素质量比=64:71,而KCl中K、Cl质量比=39:35.5=78:71,BaCl2中Ba、Cl元素质量比=137:71,ZnCl2中Zn、Cl元素质量比=65:71,CaCl2中Ca、Cl元素质量比=40:71,可得其中只有氯化钙中氯元素的质量分数大于氯化铜,故氯化铜中杂质应为氯化钙;
答案:氯化钙
CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2
135 287
13.5g x
| 135 |
| 287 |
| 13.5g |
| x |
x=28.7g.
由计算可知,实际生成的沉淀29g>假设13.5g全部是氯化铜时生成的沉淀28.7g.
如果多生成沉淀的话,则应该样品中的Cl的离子数应该是比纯的CuCl2含有的Cl离子数多,相同质量的物质中含有的离子多的话,应该是杂质中含氯离子的那个物质的相对分子质量应该比铜小.因此可以这么说杂质中的氯元素的质量分数比CuCl2中氯元素的质量分数大.氯化铜中铜、氯元素质量比=64:71,而KCl中K、Cl质量比=39:35.5=78:71,BaCl2中Ba、Cl元素质量比=137:71,ZnCl2中Zn、Cl元素质量比=65:71,CaCl2中Ca、Cl元素质量比=40:71,可得其中只有氯化钙中氯元素的质量分数大于氯化铜,故氯化铜中杂质应为氯化钙;
答案:氯化钙
点评:本题主要考查学生灵活运用化学方程式和元素的质量分数解答问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
下列实验操作,错误的是( )
A、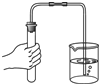 |
B、 |
C、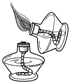 |
D、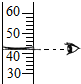 |

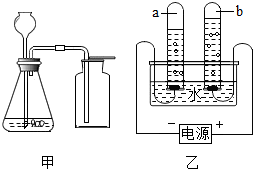 初中教材中可采用多种方法制取氧气.
初中教材中可采用多种方法制取氧气.
 A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
