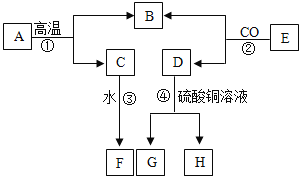
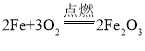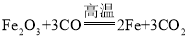题目内容
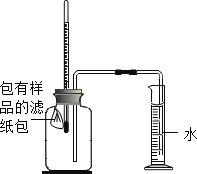
【题目】实验室用10%氢氧化钠溶液进行水的电解实验。用如图装置进行水的电解实验,已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用。
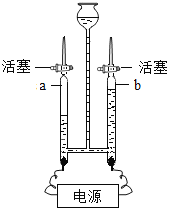
(1)开始反应前a,b两管内都充满溶液。关闭活塞,接通电源,一段时间后,两管产生的气体如图所示,则a管下方导线应接电源的______极(填“正”或“负”)。用______验证b管中的气体,写出电解水的化学符号表达式:______。该反应的基本反应类型为______ 。
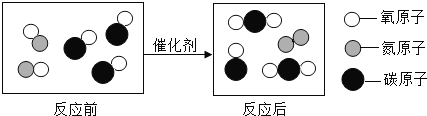
(2)该化学变化过程中的最小微粒是______,这个实验说明水是由______和______组成的。
(3)电解后溶液的溶质质量分数______10%(填“<”、“=”或“>”)
【答案】负 带火星的木条 ![]() 分解反应 氢原子、氧原子 氢元素 氧元素 >
分解反应 氢原子、氧原子 氢元素 氧元素 >
【解析】
(1)在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,故a管下方导线应接电源的负极;
B管产生的气体是氧气,故用带火星的木条可以验证b管中的气体(氧气),这是因为氧气能使带火星的木条复燃;
水在通电的条件下反应生成氢气和氧气,该反应的化学符号表达式:![]() ,该反应符合“一变多”的特点,属于分解反应。故填:负;带火星的木条;
,该反应符合“一变多”的特点,属于分解反应。故填:负;带火星的木条;![]() ;分解反应。
;分解反应。
(2)原子是化学变化中的最小粒子,故该化学变化过程中的最小微粒是氢原子和氧原子,根据质量守恒定律,化学反应前后,元素的种类不变,故这个实验说明水是由氢元素和氧元素组成的。故填:氢原子、氧原子;氢元素;氧元素。
(3)电解后,溶剂质量减小,溶液的质量减小,溶质质量不变,故溶质质量分数大于10%。故填:>。

 阅读快车系列答案
阅读快车系列答案【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学对该气体的成分进行如下探究:
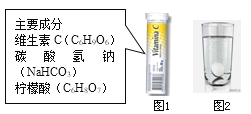
(猜想与假设)小华说:该气体可能是CO2、O2、CO、H2、N2。
(1)小明说:不可能含有N2,因为_____。
(2)小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO_____。该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
(进行实验)
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(得出结论)(3)由实验①可知,该气体中肯定含有_____,写出该反应的化学方程式_____。
(4)由实验②_____(填“能”或“不能”)确定该气体中不含氧气,理由是_____。
【题目】世界上每年因锈蚀而报废的金属设备和材料高达产量的20%~40%,某实验小组对铁的锈蚀和铁锈的成分进行如下探究。
(一)如图所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进入广口瓶。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表
序号 | 样品 | 量筒起始读数mL | 量筒最终读数mL | 所需时间/min |
① | 1g铁粉、0.2g碳和10滴水 | 100 | 72 | 约120 |
② | 1g铁粉、0.2g碳、10滴水和少量NaCl | 100 | 72 | 约70 |
③ | -- | -- | -- | -- |
(1)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是______(填“放热”或吸热”)过程。
(2)实验①和②说明NaCl可以______(填“加快”或“减慢”)铁锈蚀的速率。
(3)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成是______。
(二)为探究铁锈的成分,用如图所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全)。
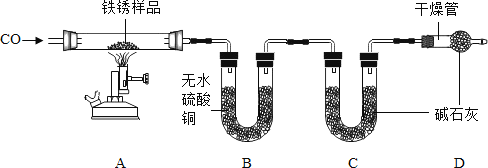
查阅资料:无水硫酸铜吸水会由白色变为蓝色,碱石灰既能吸水也能吸收CO2。
(4)该装置有一个明显缺陷是______。
(5)加热前,先通入CO一段时间,目的是______;将铁锈样品加热,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有______元素,从而推断出空气中的______参加了铁生锈反应。
(6)若将铁锈的成分表示为FexOynH2O,为了准确测定该成分,除要称量铁锈样品的质量外,还需要测定装置______(填标号)反应前后的质量。若缺少装置D,则测算出的x:y值将______(填“偏大”“偏小”或“无影响”)