题目内容
(2011?眉山)某校化学兴趣小组在老师指导下探究孔雀石(一种铜矿石)的组成元素.他们取50克孔雀石粉末,在密闭容器中加热,观察到孔雀石分解过程中有水和能使澄清石灰水变浑浊的气体产生,绿色的孔雀石逐渐变为黑色粉末(假设:孔雀石中的杂质不反应,生成的二氧化碳全部被石灰水吸收).在此过程中他们测定了五次,相关数据如下表:| 测定次数 | 生成沉淀的质量(g) | 生成水的质量(g) |
| 1 | 5 | 0.9 |
| 2 | 10 | 1.8 |
| 3 | X | 2.7 |
| 4 | 20 | 3.6 |
| 5 | 20 | 3.6 |
请分析数据,回答下列问题:
(1)组成孔雀石的元素有______.
(2)表中“X”的值为______g.
(3)实验最终生成二氧化碳的质量是多少克(写出计算过程)?
【答案】分析:从题目中我们可以看出所发生的反应是:①碱式碳酸铜分解产生的②碱式碳酸铜分解产生的二氧化碳与石灰水的反应:实验最终生成二氧化碳的质量,分析表格中所给数据,我们可以看出沉淀的质量是以5g为单位递增的,所以第三次的测定数据应该是15g,到第四次测定时是20g沉淀,第五次仍然是20g说明第四次测定时碱式碳酸铜已经分解完毕,同时二氧化碳与石灰水的反应也已经完成.那么我们就可以根据第四次所测得的数据进行求算了.
解答:解:(1)根据物质的组成元素,我们从碱式碳酸铜的化学式中可以得到它的组成为:Cu、C、O、H
(2)分析表格中所给数据,我们可以看出沉淀的质量是以5g为单位递增的,所以第三次的测定数据应该是15g,故答案应为:15
(3)解:经分析表中数据可知,在第四次测定时碱式碳酸铜已分解完毕此时产生沉淀的质量为20g.
设实验最终生成二氧化碳的质量为x,则:
CO2+Ca(OH)2═CaCO3↓+H2O
44 100
X 20g
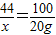
解得:x=8.8g
答:实验最终生成二氧化碳的质量是8.8g.
点评:解这类题的关键是根据题意写出发生反应的化学方程式,然后再根据题意来分析出已知量、未知量来进行解答.本题也可以根据碱式碳酸铜分解的化学方程式,以水的质量来进行求算.
解答:解:(1)根据物质的组成元素,我们从碱式碳酸铜的化学式中可以得到它的组成为:Cu、C、O、H
(2)分析表格中所给数据,我们可以看出沉淀的质量是以5g为单位递增的,所以第三次的测定数据应该是15g,故答案应为:15
(3)解:经分析表中数据可知,在第四次测定时碱式碳酸铜已分解完毕此时产生沉淀的质量为20g.
设实验最终生成二氧化碳的质量为x,则:
CO2+Ca(OH)2═CaCO3↓+H2O
44 100
X 20g
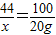
解得:x=8.8g
答:实验最终生成二氧化碳的质量是8.8g.
点评:解这类题的关键是根据题意写出发生反应的化学方程式,然后再根据题意来分析出已知量、未知量来进行解答.本题也可以根据碱式碳酸铜分解的化学方程式,以水的质量来进行求算.

练习册系列答案
相关题目
(2011?眉山)某同学对酸碱盐的知识进行了以下的梳理.
(1)填写下表空格中的化学式:
反思:根据以上盐中的金属元素的排列,可以得出是依据顺序归纳整理的.
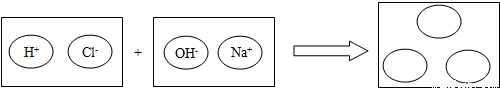
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了下图.请你在右边的圆圈中填入适当的化学式或离子符号:
(3)此同学通过查阅资料,发现许多反应都有盐类物质生成(如图).比如①用稀硫酸除铁锈;②古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液.请从①、②中任选一个,写出反应的化学方程式:.

(1)填写下表空格中的化学式:
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | ZnCl2 | FeCl2 | CuCl2 |
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了下图.请你在右边的圆圈中填入适当的化学式或离子符号:

(3)此同学通过查阅资料,发现许多反应都有盐类物质生成(如图).比如①用稀硫酸除铁锈;②古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液.请从①、②中任选一个,写出反应的化学方程式:.


