题目内容
【题目】海洋蕴藏着丰富的资源。我国国产航母001A已经建成下水,即将海试。她将用于保护我国海洋国土安全。下列有关说法正确的是( )

A. 海洋幅原辽阔,远海是倾倒垃圾废物的理想场所
B. 工业上用海水晒盐没有把海水晒干,原因是防止海水中氯化镁等可溶性杂质随氯化钠一起结晶析出
C. 海洋中拥有丰富的渔业资源,可以大肆捕捞各种海鲜
D. 可以用海水提炼金属镁是因为海水中含有金属镁
【答案】B
【解析】
A、垃圾废物直接倾倒到海中,会污染海水,从而使海洋生物受到损害,不利于保护海洋环境,故说法错误;
B、海水晒盐没有把海水直接蒸发干,目的是防止海水中的氯化镁等可溶性杂质随氯化钠一起结晶析出,故说法正确;
C、海洋中虽然拥有丰富的渔业资源,如果大肆捕捞各种海鲜,生态平衡就会受到破坏,有些生物可能濒临灭绝的危险,故说法错误;
D、金属镁是由海水中的MgCl2提炼出来的,故说法错误。
故选B。

 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案【题目】某化学活动小组合作学习氢氧化钠和氢氧化钙的相关知识。如表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
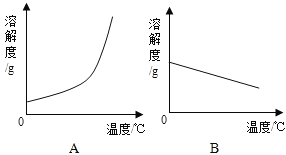
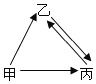
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是_____(填“A”或“B”)。
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入适量氢氧化钙②升高温度③降低温度④加入水⑤蒸发水后再恢复到原温度⑥加入适量生石灰。
其中措施在原理上正确的是_____(填字母)
A ②④⑥ B ③④ C ①②⑤⑥ D ①②⑤
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体。这时溶液的质量分数为_____
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____(填“偏大”或“偏小”“不受影响”)。
(5)可鉴别氢氧化钠溶液和澄清石灰水的一个化学反应方程式为_____。