题目内容
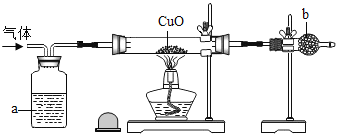
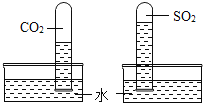
【题目】根据如图所示实验分析得出的结论中,不正确的是()
A | B | C | D |
|
|
|
|
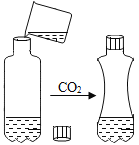
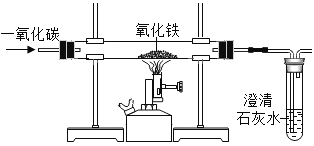
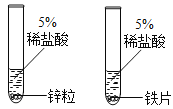
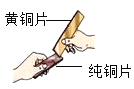
二氧化碳与水反应生成碳酸 | 一氧化碳能还原氧化铁 | 金属锌的活动性比铁的活动性强 | 黄铜硬度比纯铜大 |
A.AB.BC.CD.D
【答案】A
【解析】
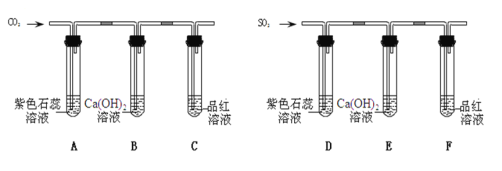
A、二氧化碳能溶于水,使瓶内压强减小,使塑料瓶变瘪,但是是否会有产物碳酸生成,需用酸碱指示剂检验,符合题意;
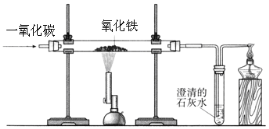
B、一氧化碳能与氧化铁在高温的条件下反应生成铁和二氧化碳,氧化铁为红色,铁为黑色,二氧化碳能使澄清石灰水变浑浊,故观察到红色固体变成黑色,石灰水变浑浊,说明一氧化碳能还原氧化铁,不符合题意;
C、相同形状、大小的锌片和铁片,放入等浓度的稀盐酸中,锌片表面产生气泡的速率比铁片快,说明锌比铁活泼,不符合题意;
D、黄铜片和铜片相互刻画,铜片上能够留下痕迹,说明黄铜的硬度大于铜的硬度,不符合题意。
故选A。

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目