题目内容
【题目】用金属铁制备自来水新型消毒、净水剂Na2FeO4的流程如下,请回答下列问题:

(1)固体B中的物质是 _______;Na2FeO4属于 ______(填“酸”、“碱”、“盐”、“氧化物”).
(2)操作Ⅰ的名称是________;该操作能使A、B分离的原因是_________.
(3)反应②的基本反应类型为:_______;反应③的化学方程式为:________.
(4)溶液C中的溶质组成存在_________种可能性.
【答案】Fe和Cu 盐 过滤 A是液体,B是固体(合理皆可) 复分解反应 2Fe(OH)2+H2O2=2Fe(OH)3 三
【解析】
(1)由反应的流程可知,过量的铁粉与硫酸铜反应,生成了硫酸亚铁和铜,由于铁是过量的,在过滤后得到的固体B是Cu,Fe的混合物;Na2FeO4是金属离子和酸根离子构成的化合物,属于盐。
故填:Fe和Cu;盐;
(2)由上述反应①得到是固液的混合物,要将固液分开,应进行的操作是过滤。
故填:过滤;A是液体,B是固体(合理皆可);
(3)反应②是硫酸亚铁与氢氧化钠反应生成氢氧化亚铁和硫酸钠,反应的方程式是:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4,该反应是两种化合物交换成分生成另外两种化合物,属于复分解反应;反应③是氢氧化亚铁被过氧化氢氧化为氢氧化铁,方程式是:2Fe(OH)2+H2O2=2Fe(OH)3。
故填:复分解反应;2Fe(OH)2+H2O2=2Fe(OH)3;
(4)若氢氧化钠溶液与硫酸亚铁溶液恰好完全反应,所得溶液中只有一种溶质——硫酸钠;若氢氧化钠过量,则有两种溶质﹣﹣硫酸钠和氢氧化钠;若硫酸亚铁过量,则有两种溶质﹣﹣硫酸钠和硫酸亚铁。
故填:三。

 阅读快车系列答案
阅读快车系列答案【题目】水是生命的源泉,也是不可缺少的资源。
(1)某矿泉水的主要矿物质成分及含量如下表:
成分 | Ca | K | Mg | Na |
含量(mg/L) | ≥4 | ≥0.4 | ≥0.5 | ≥0.8 |
这里含有的Ca、K、Mg、Na是指_____(填“单质、元素、分子或原子”)。
(2)自然界中的水含有许多可溶性和不溶性杂质,通过多种途径都可以使水得到净化,下图是自来水厂净化水过程示意图。
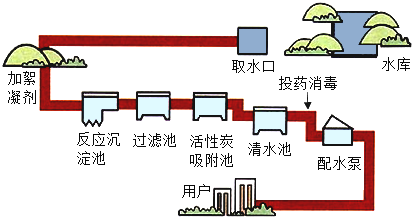
(Ⅰ)自来水厂使用的净化水的方法主要有:沉淀、_____、_____、消毒等。
(Ⅱ)生活中,通过煮沸既能降低自来水的硬度,又能杀菌消毒,但也会造成壶中出现水垢,原因是烧水时自来水中的少量Ca(HCO3)2发生分解,生成难溶性的碳酸钙和二氧化碳等物质,请写出Ca(HCO3)2受热分解的化学方程式_____。
(Ⅲ)下列做法会造成水体污染的是_____(填序号)。
A 工业废水直接排放
B 生活污水集中处理后排放
C 禁止使用含磷洗衣粉
D 大量使用化肥、农药
(3)电解水实验揭示了水的组成,理论依据是_____。