题目内容
【题目】托盘天平两盘烧杯中分别装有100g溶质质量分数为7.3%的稀盐酸,天平平衡。分别向两个烧杯中加入下列物质,充分反应后天平仍然平衡的是( )
A. 左盘5.6g铁 右盘6.5g锌
B. 左盘2.8g铁 右盘2.8g镁
C. 左盘4.8g镁 右盘4.6g氧化镁
D. 左盘10g碳酸钙 右盘10g碳酸镁
【答案】CD
【解析】
100g7.3%的稀盐酸中溶质的质量为100g×7.3%=7.3g;
A、
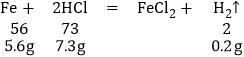

左盘恰好完全反应,增重的质量为:5.6g﹣0.2g=5.4g;
右盘恰好完全反应,增重的质量为:6.5g﹣0.2g=6.3g,所以天平不平衡,故A错误;
B、


左盘Fe完全反应,增重的质量为:2.8g﹣0.1g=2.7g;
右盘盐酸完全反应,增重的质量为:2.8g﹣0.2g=2.6g,所以天平不平衡,故B错误;
C、

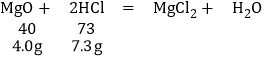
左盘盐酸完全反应,增重的质量为:4.8g﹣0.2g=4.6g;
右盘盐酸完全反应,增重的质量为4.6g,天平平衡,故C正确;
D、

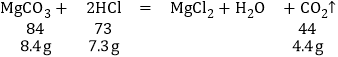
由化学方程式可知,碳酸镁过量,碳酸钙完全反应,所依据盐酸可以求出生成的二氧化碳质量相等,所以反应后烧杯中增加质量相等,天平平衡,故D正确。
故选:CD。

【题目】某化学兴趣小组的同学向氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象。
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量。
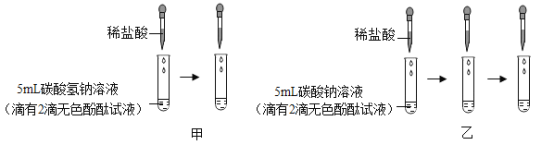
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告。
同学 | 实验操作 | 现象 | 结论 |
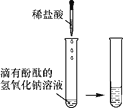
甲 |
| 溶液由红色变成________ | 氢氧化钠与盐酸发生了化学反应,反应的化学方程式为__________ |
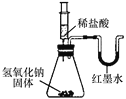
乙 |
| U形玻璃管中________边的红墨水液面下降(所加稀盐酸的体积忽略不计) | 氢氧化钠与盐酸发生了化学反应 |
丙 | 用________测定氢氧化钠溶液的pH;向其中滴加足量的稀盐酸后,再测定溶液的pH | 最后溶液的pH________(填“≥7”“≤7”或“不变”) | 氢氧化钠与盐酸发生了化学反应 |
【评价反思】你认为实验设计方案不合理的同学是________,理由是______________________________。