题目内容
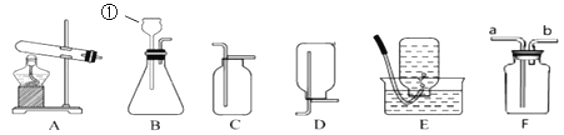
【题目】铁是生产、生活中应用很广泛的一种金属,下列是与铁的性质有关的部分实验图,
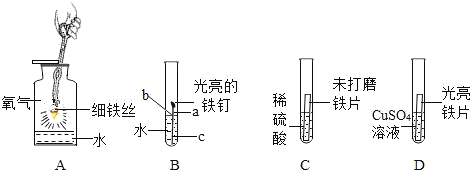
请回答下列问题。
(1)A中细铁线燃烧生成黑色固体的化学方程式是_____。
(2)B中铁钉最易生锈的部位是_____ (填“a”、“b”或“c”)。
(3)C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内反应的化学方程式是_____。
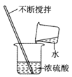
(4)D中反应一段时间后,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反应前相比_____(填“增大”、“不变”或“减小”)。化学方程式为_____。
【答案】3Fe+2O2![]() Fe3O4 b Fe2O3+6HCl═2FeCl3+3H2O 减小 Fe+CuSO4═FeSO4+Cu
Fe3O4 b Fe2O3+6HCl═2FeCl3+3H2O 减小 Fe+CuSO4═FeSO4+Cu
【解析】
(1)铁与氧气在点燃的条件下反应生成四氧化三铁,反应的化学方程式为:![]() ;
;
(2)铁与氧气、水共存时最易生锈,所以B中铁钉最易生锈的部位是b;
(3)铁片表面的铁锈主要成分是氧化铁,氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
(4)铁和硫酸铜反应产生硫酸亚铁和铜,由反应的方程式Fe+CuSO4=FeSO4+Cu可知,每56份质量的铁参加反应生成了64份质量的铜,试管内固体质量比反应前增大,试管内溶液质量与反应前相比减小。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案【题目】阅读下面科普短文。
纯净的臭氧(O3)在常温下是天蓝色的气体,有难闻的鱼腥臭味,不稳定,易转化为氧气。它虽然是空气质量播报中提及的大气污染物,但臭氧层中的臭氧能吸收紫外线,保护地面生物不受伤害。而且近年来臭氧的应用发展较快,很受人们的重视。
生产中大量使用的臭氧通常由如图所示方法制得。
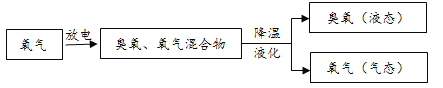
臭氧处理饮用水。早在19世纪中期的欧洲,臭氧已被用于饮用水处理。由于臭氧有强氧化性,可以与水中的有害化合物(如硫化铅)发生反应,处理效果好,不会产生异味。
臭氧做漂白剂。许多有机色素的分子遇臭氧后会被破坏,成为无色物质。因此,臭氧可作为漂白剂,用来漂白麻、棉、纸张等。实践证明,臭氧的漂白作用是氯气的15倍之多。
臭氧用于医用消毒。与传统的消毒剂氯气相比,臭氧有许多优点,如表1所示。
表1 臭氧和氯气的消毒情况对比
消毒效果 | 消毒所需时间(0.2mg/L) | 二次污染 | 投资成本 (900m3设备) | |
臭氧 | 可杀灭一切微生物,包括细菌、病毒、芽孢等 | <5min | 臭氧很快转化为氧气,无二次污染,高效环保 | 约45万元 |
氯气 | 能杀灭除芽孢以外的大多数微生物,对病毒作用弱 | >30min | 刺激皮肤,有难闻气味,对人体有害,有二次污染、残留,用后需大量水冲洗 | 约3~4万元 |
依据文章内容回答下列问题。
(1)氧气(O2)和臭氧(O3)沸点比较低的是_____。
(2)臭氧处理饮用水时,利用了臭氧的_____(填“物理”或“化学”)性质。
(3)依据表1信息,为了快速杀灭病毒,应选择的消毒剂是_____。
(4)下列关于臭氧的说法中,正确的是_____(填序号)。
A 臭氧的漂白作用比氯气强
B 由氧气制得臭氧的过程中,既有物理变化也有化学变
C 臭氧在生产生活中有很多用途,对人类有益无害
D 臭氧稳定性差,不利于储存,其应用可能会受到限制