题目内容
【题目】常温下,在一定量的水溶液中,氯酸钾易达到饱和状态。在工业上可通过如下工艺流程制得。

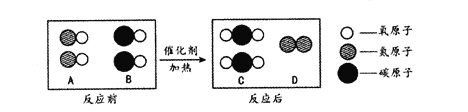
(1)反应I中,通电时发生的反应方程式为:NaC1+3X![]() NaC1O3+3H2↑,则X的化学式为___________。
NaC1O3+3H2↑,则X的化学式为___________。
(2)反应Ⅱ的反应方程式为:______________________。
(3)该流程中可以循环利用的物质是___________,从微观角度探析该物质是由___________构成(用化学用语表示)。
【答案】H2O NaClO3+KCl═KClO3↓+NaCl 氯化钠 Na+和Cl﹣
【解析】
(1)反应Ⅰ中,通电时发生的反应方程式为NaCl+3X![]() NaClO3+3H2↑,反应后有钠原子1个,氯原子1个,氧原子3个,氢原子6个;反应前有钠原子1个,氯原子1个;缺少 氧原子3个,氢原子6个,这些原子分布在3个X分子中,所以每个X分子含有两个氢原子和一个氧原子,则X的化学式为 H2O;
NaClO3+3H2↑,反应后有钠原子1个,氯原子1个,氧原子3个,氢原子6个;反应前有钠原子1个,氯原子1个;缺少 氧原子3个,氢原子6个,这些原子分布在3个X分子中,所以每个X分子含有两个氢原子和一个氧原子,则X的化学式为 H2O;
(2)根据流程图可知,反应Ⅱ,是氯酸钠溶液与氯化钾反应生成氯酸钾固体和氯化钠,化学方程式为:NaClO3+KCl═KClO3↓+NaCl;
(3)氯化钠在反应过程中,既是反应物,也是生成物,该转化中可以循环利用的物质是氯化钠NaCl,氯化钠是由钠离子和氯离子构成的,其离子符号为Na+和Cl﹣。

练习册系列答案
相关题目