题目内容
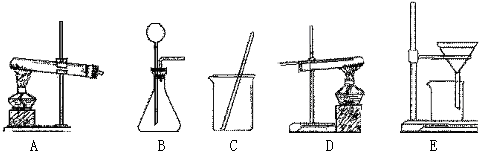
采用两种方法制取铜,现有锌、氧化铜、稀硫酸三种物质及下列实验装置供选择.(1)第一种方法的实验过程中有蓝色溶液产生,应选用下面装置中的______,写出此现象的化学方程式______.
(2)第二种方法应选用下面装置中的______和 D.
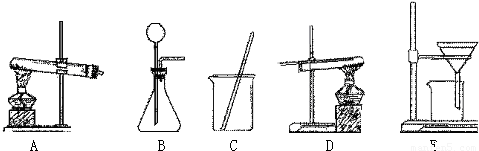
(3)在第二种方法制取的铜中,可能存在的黑色杂质是______.
(4)在以上两个设计方法中,你认为第______种方法操作更合理、更简便.
【答案】分析:根据锌、氧化铜、稀硫酸三种物质之间的反应规律分析解答,氧化铜能与稀硫酸反应生成硫酸铜,锌能置换硫酸铜溶液中的铜;锌能与稀硫酸反应生成氢气,氢气能置换氧化铜中的铜.
解答:解:(1)用锌、氧化铜、稀硫酸三种物质制取铜,实验过程中有蓝色溶液产生,因此方法是将氧化铜与硫酸反应生成硫酸铜,然后将锌粒与硫酸铜反应置换出铜,采用过滤法即可得到铜.故选用的装置应为CE;化学方程式为
CuO+H2SO4=CuSO4+H2O
(2)第二种方法用到装置D氢气还原氧化铜,因此实验方案是用锌粒与稀硫酸反应生成氢气,氢气再还原氧化铜得到金属铜,因此用到的装置还有B,固液常温下制取气体的装置;
(3)用氢气还原氧化铜的方法制取时可能由于氧化铜未完全反应而留在反应后的固体中,故答案为氧化铜;
(4)以上两个方法中,第1种方法操作更合理,简便,得到的铜不含有杂质.
故答案为:(1)C E CuO+H2SO4=CuSO4+H2O 用HCl和HNO3都可以
(2)B (3)CuO (4)1
点评:明确单质、氧化物、酸碱盐之间的反应规律是解答制备物质题的关健
解答:解:(1)用锌、氧化铜、稀硫酸三种物质制取铜,实验过程中有蓝色溶液产生,因此方法是将氧化铜与硫酸反应生成硫酸铜,然后将锌粒与硫酸铜反应置换出铜,采用过滤法即可得到铜.故选用的装置应为CE;化学方程式为
CuO+H2SO4=CuSO4+H2O
(2)第二种方法用到装置D氢气还原氧化铜,因此实验方案是用锌粒与稀硫酸反应生成氢气,氢气再还原氧化铜得到金属铜,因此用到的装置还有B,固液常温下制取气体的装置;
(3)用氢气还原氧化铜的方法制取时可能由于氧化铜未完全反应而留在反应后的固体中,故答案为氧化铜;
(4)以上两个方法中,第1种方法操作更合理,简便,得到的铜不含有杂质.
故答案为:(1)C E CuO+H2SO4=CuSO4+H2O 用HCl和HNO3都可以
(2)B (3)CuO (4)1
点评:明确单质、氧化物、酸碱盐之间的反应规律是解答制备物质题的关健

练习册系列答案
相关题目