题目内容
【题目】如图为KNO3的溶解度曲线图,现有M状态下的KNO3溶液65g,若要将该溶液经过处理后,刚好得到该温度下的饱和溶液,下列处理方法正确的是( ) 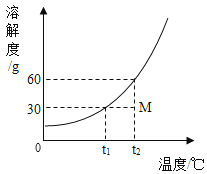
A.在t2℃时,将65g溶液倒出去32.5g
B.将65g溶液蒸发掉32.5g的水,再冷却到t2℃
C.将65g溶液的温度从t2℃降低到t1℃
D.在t2℃时,向65g溶液中加入15gKNO3固体并充分溶解
【答案】D
【解析】A、将65g溶液倒出去32.5g后溶液的质量分数不变,仍是不饱和溶液,故选项错误;
B、原65g溶液中含有65×![]() =15g的KNO3固体,蒸发掉32.5g的水,再冷却到t2℃后,溶质比溶液=
=15g的KNO3固体,蒸发掉32.5g的水,再冷却到t2℃后,溶质比溶液=![]() >
>![]() ,所以有固体析出,不能恰好得到t2℃下的饱和溶液,故选项错误;
,所以有固体析出,不能恰好得到t2℃下的饱和溶液,故选项错误;
C、题干要求刚好得到该温度下的饱和溶液,故不能改变温度,故选项错误;
D、原65g溶液中含有65× ![]() =15g的KNO3固体,加入15gKNO3固体并充分溶解后,溶质比溶液=
=15g的KNO3固体,加入15gKNO3固体并充分溶解后,溶质比溶液=![]() =
=![]() ,所以恰好得到该温度下的饱和溶液,故选项正确;故选D.
,所以恰好得到该温度下的饱和溶液,故选项正确;故选D.
【考点精析】利用固体溶解度曲线及其作用对题目进行判断即可得到答案,需要熟知1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

练习册系列答案
相关题目
【题目】在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下表:下列说法不正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 5 | 2 | 20 | 22 |
反应后质量/g | 待测 | 11 | 28 | 5 |
A. 乙、丙变化的质量比为9:8 B. 甲可能是该反应的催化剂
C. 该反应是分解反应 D. 反应后甲的质量为0g
