题目内容
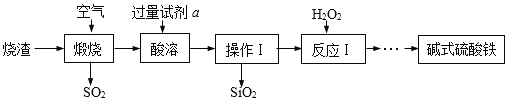
【题目】石灰石是我省的主要矿产之一。学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g。平均生成4份,进行实验,结果如下:

(1)哪几次反应中矿石有剩余?________________。
(2)上表中m的数值是________________________。
(3)试计算这种石灰石矿中碳酸钙的质量分数。
【答案】(1)第三、四次 (2)4.4 (3)80%
【解析】(1)由题中信息可知,每5g样品完全反应生成1.76g二氧化碳,所以样品15g时只生成4.4g二氧化碳,说明碳酸钙已经有剩余,所以第三、四次矿石有剩余(2)第四次反应掉的碳酸钙与第三次相同,生成二氧化碳的质量也相同,均为4.4 g (3)设石灰石矿中碳酸钙的质量为x;CaCO3 +2HCl ==CaCl2+ CO2↑ + H2O
100 44
x 1.76g
100/x=44/4.4g x=4g
石灰石矿中碳酸钙的质量分数为4g÷5g×100%=80%
答:略

【题目】甲、乙两种物质的溶解度曲线如图.
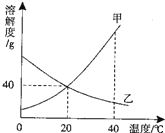
(1)20℃时,甲物质的溶解度为40 ______g;
(2)欲将40℃时,乙物质的饱和溶液变为不饱和溶液,可采用的方法是加水或降温 ____________;
(3)40℃时,将甲、乙两物质的饱和溶液各100g,分别降温到20℃,所得甲物质溶液的质量< _______(选填“>”或“=”或“<”)乙物质溶液的质量.
(4)下表为KCl在不同温度下的溶解度:
温度╱℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度╱g | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 |
①由上表可推测KCl溶解度随温度的升高而________增大(填“增大”或“减小”).
②在10℃时,向100g水中加入40gKCl固体,充分混合溶解后所得溶液为________饱和(填“饱和”或“不饱和”)溶液,此过程中的玻璃棒的作用为__________加快溶解速率;将其温度升高到40℃时,若不考虑溶剂的变化,则该溶液中溶质的质量分数为28.6% _________(计算结果精确到0.1%).
【题目】液化石油气作为燃料,已普遍进入城乡家庭,它是含有下列物质的混合物,在常压下,这些物质的沸点如下表所示:
物质名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
沸点/℃ | -88.6 | -42.2 | -0.5 | 36.1 | 69.2 |
在常温下使用至无气体放出时,钢瓶中常剩余的物质是:
A. 戊烷和己烷 B. 乙烷和丙烷
C. 只有己烷 D. 乙烷、丙烷和丁烷