题目内容
实验室有一包失去标签的白色同体物质,只知道是碳酸钠、氧化钙、氢氧化钠中的一种.为了确定其组成,某同学大胆假设并设计实验进行探究.
[查阅资料]碳酸钠与氢氧化钙溶液反应生成氧氧化钠和碳酸钙沉淀.
[提出假设]假设①:白色固体是碳酸钠;假设②:白色固体是氧化钙;假设③:白色固体是氢氧化钠.
[实验与分析]根据假没.通过实验及分析,可作出如下判断(填表):
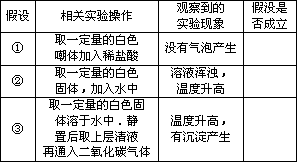
| 假设 | 相关实验操作 | 观察到的实验现象 | 假没是否成立 |
| ① | 取一定量的白色固体加入稀盐酸 | 没有气泡产生 | ________ |
| ② | 取一定量的白色固体,加入水中 | 溶液浑浊,温度升高 | ________ |
| ③ | 取一定量的白色固体溶于水中.静置后取上层清液再通入二氧化碳气体 | 温度升高,有沉淀产生 | ________ |
不成立 成立 不成立 有沉淀产生 CaO+H2O═Ca(OH)2 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH 过滤 Na2CO3,NaOH
分析:根据物质的性质进行分析,碳酸钠能与盐酸反应生成二氧化碳,氧化钙与水反应生成氢氧化钙的反应是放热反应,二氧化碳能使澄清石灰水变浑浊,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,分离不溶性固体和可溶性固体可以使用过滤的方法.
解答:实验与分析:碳酸钠能与盐酸反应生成二氧化碳,加入盐酸没有气泡产生,则猜想①不成立,氧化钙与水反应生成氢氧化钙放出大量的热,取一定量的白色固体,加入水中溶液浑浊且温度升高,说明猜想②成立,取一定量的白色固体溶于水中.静置后取上层清液再通入二氧化碳气体,温度升高,有沉淀生成,则固体不是氢氧化钠,故猜想③不成立,固体:不成立,成立,不成立;
拓展延伸:白色固体是混有少量氧化钙的碳酸钠,先将适量此混合物溶于足量水中,则氧化钙与水反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙沉淀,故会看到有沉淀产生,要分离不溶性固体和可溶性固体可以使用过滤的方法,氧化钙量少,则反应生成的氢氧化钙的量少,与碳酸钠反应后碳酸钠有剩余,将分离后的溶液蒸干,得到的固体物质是 Na2CO3,NaOH,故填:有沉淀产生,CaO+H2O═Ca(OH)2 Ca(OH)2+Na2CO3═CaCO3↓+2 NaOH,过滤,Na2CO3,NaOH.
点评:本题考查了物质成分的探究,完成此题,可以依据物质的性质进行,要熟记物质间反应时的实验现象,以便灵活应用.
分析:根据物质的性质进行分析,碳酸钠能与盐酸反应生成二氧化碳,氧化钙与水反应生成氢氧化钙的反应是放热反应,二氧化碳能使澄清石灰水变浑浊,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,分离不溶性固体和可溶性固体可以使用过滤的方法.
解答:实验与分析:碳酸钠能与盐酸反应生成二氧化碳,加入盐酸没有气泡产生,则猜想①不成立,氧化钙与水反应生成氢氧化钙放出大量的热,取一定量的白色固体,加入水中溶液浑浊且温度升高,说明猜想②成立,取一定量的白色固体溶于水中.静置后取上层清液再通入二氧化碳气体,温度升高,有沉淀生成,则固体不是氢氧化钠,故猜想③不成立,固体:不成立,成立,不成立;
拓展延伸:白色固体是混有少量氧化钙的碳酸钠,先将适量此混合物溶于足量水中,则氧化钙与水反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙沉淀,故会看到有沉淀产生,要分离不溶性固体和可溶性固体可以使用过滤的方法,氧化钙量少,则反应生成的氢氧化钙的量少,与碳酸钠反应后碳酸钠有剩余,将分离后的溶液蒸干,得到的固体物质是 Na2CO3,NaOH,故填:有沉淀产生,CaO+H2O═Ca(OH)2 Ca(OH)2+Na2CO3═CaCO3↓+2 NaOH,过滤,Na2CO3,NaOH.
点评:本题考查了物质成分的探究,完成此题,可以依据物质的性质进行,要熟记物质间反应时的实验现象,以便灵活应用.

练习册系列答案
相关题目
已知在溶液中氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠.现实验室有一瓶失去标签但密封保存良好的白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙.为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动.
(1)提出假设:假设①白色粉末是碳酸钠;假设②白色粉末是氧化钙;假设③白色粉末是氢氧化钙.
(2)设计实验,通过实验分析进行判断并填空:
| 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
| 取一定量粉末加入稀盐酸 | 没有气体产生 | 假设① |
| 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 假设② |
| 假设③ |
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是______;若将反应后的混合物进行固液分离,分离的方法是______;再将分离后的溶液蒸干,得到的固体物质是______、______(填化学式).