题目内容
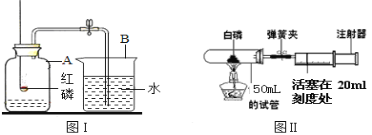
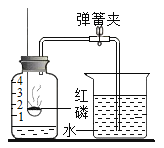
【题目】(1)测定空气中氧气体积分数的实验装置如右图所示。在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号。用弹簧夹夹紧乳胶管。点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧。
①写出红磷在空气中燃烧的文字表达式:____
②待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处。由此得出的实验结论是:_____。
③红磷熄灭后,集气瓶内剩下的气体主要是氮气,请写出该气体在本实验中体现出来的性质是:___(任写一条)
(2)同学们在实验后发现气体减少的体积小于1/5,请你帮助这位同学找出两种可能造成这样结果的原因:(写两条)①____;②_____
【答案】![]() 氧气体积约占空气体积的五分之一 氮气不燃烧不支持燃烧;氮气不易溶于水(任写一条) 红磷的量不足,氧气没有耗尽 没有冷却至室温就打开了止水夹
氧气体积约占空气体积的五分之一 氮气不燃烧不支持燃烧;氮气不易溶于水(任写一条) 红磷的量不足,氧气没有耗尽 没有冷却至室温就打开了止水夹
【解析】
(1)测定空气中氧气体积分数的实验:
①红磷在空气中燃烧,红磷与氧气在点燃条件下生成五氧化二磷,反应的文字表达式为![]() ;
;
②待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处。由此得出的实验结论是:氧气体积约占空气体积的五分之一。
③红磷熄灭后,集气瓶内剩下的气体主要是氮气,在本实验中体现出来的性质是:氮气不燃烧也不支持燃烧;氮气不易溶于水(任写一条)。
(2)实验后发现气体减少的体积小于1/5,造成偏小的误差的原因有:①红磷的量不足,氧气没有耗尽;②没有冷却至室温就打开了止水夹。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】请根据下列各图中提供的信息回答问题:

(1)仪器①的名称是_______。
(2)实验室用高锰酸钾制取氧气,应选用发生装置_______(填字母序号),反应的文字表达式为________________。A与D组合制到较纯净的氧气,马明同学观察到装置D中的水变为红色,相应的改进措施是_____。若用该装置收集的氧气也不纯,原因可能是:_________(写一点)。当观察到__________的现象时,说明氧气已收集满。
(3)比较用过氧化氢溶液和用氯酸钾固体制取O2的方法,两者的共同点是____。
A发生装置相同 B都可用MnO2做催化剂 C完全反应后剩余固体的成分相同
(4)实验室制取CO2一般有六个步骤:①检查装置的气密性;②按要求装配好仪器; ③向漏斗中注入酸液;④向仪器①中放入小块的大理石;⑤用燃着的木条靠近集气瓶口验满;⑥收集气体。则正确的操作顺序是_______(填数字序号)。发生反应的文字表达式为___________。装置B、C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优点是_________。
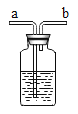
(5)若用G装置进行排空气法收集二氧化碳,检验二氧化碳已满的方法是_________;细心观察发现:G装置中的广口瓶与收集气体的集气瓶都有磨砂部分,所不同的是集气瓶的磨砂部分位于________。
A瓶底内壁 B瓶口边缘 C瓶颈内壁 D瓶底外壁
(6)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(已知:氨气密度比空气小,极易溶于水),则实验室制取氨气可选用的实验装置组合为______(填序号,在A-F中选);
(7)实验室用双氧水制氧气。某同学为研究MnO2粉末用量对双氧水分解速率的影响,做了以下实验:采用不同质量的MnO2粉末做催化剂,每次均用30mL 10%的双氧水(其他实验条件均相同),测定收集500mL氧气所用的时间,结果如表:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
MnO2用量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 |
所用时间/s | 17 | 8 | 6 | 3 | 2 | 2 | 2 | 2 | 2 |
①写出上述反应的文字表达式:_____________。
②该实验可得出的结论是___________。