题目内容
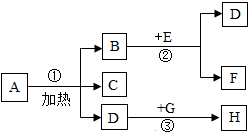 在如图转化关系中,生成物D能使带火星的木条复燃,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均没有改变.
在如图转化关系中,生成物D能使带火星的木条复燃,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均没有改变.(1)图中A是
高锰酸钾
高锰酸钾
,B是二氧化锰
二氧化锰
,D是氧气
氧气
,H是二氧化碳
二氧化碳
.(2)属于化合反应的是
③
③
(填序号).分析:解题关键,找准解题的突破口,并从突破口出发,探求知识间的内在联系,应用多种思维方式,进行严密的分析和逻辑推理,推出符合题意的结果.本题的突破口为“D能使带火星的木条复燃,H能使澄清石灰水变浑浊”,所以D为氧气,H为二氧化碳;在反应②中,B的质量和化学性质均不改变,则B为该反应的催化剂,据此分析解答即可.
解答:解:由题意可知,D能使带火星的木条复燃为氧气,H能使澄清石灰水变浑浊为二氧化碳,在②的反应前后B的质量和化学性质都不改变,所以B是催化剂,氧气和G点燃会生成二氧化碳,所以G是一氧化碳或碳,A加热会生成氧气和一种催化剂,所以A就是高锰酸钾,B就是二氧化锰,C就是锰酸钾,二氧化锰和E常温会生成氧气和F,所以E是过氧化氢,F是水.
(1)由以上推断知:A是高锰酸钾,B是二氧化锰,D是氧气,H是二氧化碳;
(2)由图示的分析可知D+G→H,是碳或一氧化碳与氧气生成二氧化碳的过程,该反应符合“多变一”的化合反应特征,所以属化合反应,高锰酸钾受热生成锰酸钾、二氧化锰和氧气,符合分解反应的特点“一变多”,过氧化氢在二氧化锰的催化作用下生成水和氧气,符合分解反应的特点“一变多”,所以两者均属于分解反应;
故答案为:高锰酸钾;二氧化锰;氧气;二氧化碳;③;
(1)由以上推断知:A是高锰酸钾,B是二氧化锰,D是氧气,H是二氧化碳;
(2)由图示的分析可知D+G→H,是碳或一氧化碳与氧气生成二氧化碳的过程,该反应符合“多变一”的化合反应特征,所以属化合反应,高锰酸钾受热生成锰酸钾、二氧化锰和氧气,符合分解反应的特点“一变多”,过氧化氢在二氧化锰的催化作用下生成水和氧气,符合分解反应的特点“一变多”,所以两者均属于分解反应;
故答案为:高锰酸钾;二氧化锰;氧气;二氧化碳;③;
点评:解决此类图框推断题的关键是找到解题突破口,然后“顺藤摸瓜”进行顺推、逆推或顺、逆推相结合,从而得出结论;最后代入原题检验即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 在化工生产中,原料往往不能全部转化成产品.某校学生对买来的工业固体烧碱的杂质成分进行研究,他们查阅资料得知:在工业上用食盐和水配成饱和食盐水,通过电解(通电)制得烧碱溶液,再将溶液浓缩即可得到固体烧碱,通电过程中还可得到氢气和氯气(Cl2).他们推测该工业固体烧碱中可能含有碳酸钠、氯化钠,并设计了实验来验证假设.
在化工生产中,原料往往不能全部转化成产品.某校学生对买来的工业固体烧碱的杂质成分进行研究,他们查阅资料得知:在工业上用食盐和水配成饱和食盐水,通过电解(通电)制得烧碱溶液,再将溶液浓缩即可得到固体烧碱,通电过程中还可得到氢气和氯气(Cl2).他们推测该工业固体烧碱中可能含有碳酸钠、氯化钠,并设计了实验来验证假设.(1)请你帮助他们完成实验报告:
| 实验步骤 | 实验现象 | 结 论 |
| ①取样,加足量的水 | 固体完全溶解 | -- |
| ②用试管取上述试液,加入过量稀硝酸,塞上带导管的单孔塞;将导管的另一端插入 |
有 有 |
证明原固体烧碱中含有碳酸钠 |
| ③向试管中再加入硝酸银 | 有白色沉淀生成 | 证明原固体烧碱中含有 |
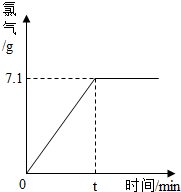
( 3 )现取100g室温下的饱和食盐水(此时质量分数约为26.5%)进行电解,当反应停止后,生成氯气的质量与时间的关系如图所示.请计算:参加反应的氯化钠的质量是多少?反应后所得烧碱溶液的质量分数是多少?(计算结果精确到0.001)
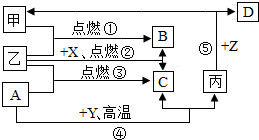 如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态.化合物D的水溶液呈浅绿色.
如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态.化合物D的水溶液呈浅绿色.
