题目内容
 根据下表回答问题.
根据下表回答问题.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)60℃时在100g水中加入100g硝酸钾固体,充分溶解后所形成的溶液是________溶液(“饱和”或“不饱和”).
(3)将上述(2)中溶液降温到20℃时,析出的晶体质量是________g.
(4)工业上将硝酸钾和氯化钠的热混合溶液(两者均己达到饱和)冷却至室温,析出晶体.
①析出的晶体中主要物质是________;
②关于剩余溶液.下列说法正确的是________(填序号);
A.只含氯化钠,不含硝酸钾
B.含有氯化钠,又含有硝酸钾,且只有硝酸钾达到饱和
C.含有氯化钠,又含有硝酸钾,且两者都达到饱和
(5)20℃时,将18克氯化钠溶解在80克水中,应至少蒸发________g 水才能形成饱和溶液.蒸发时要用到玻璃棒,其作用是________.
A.搅拌促进溶解 B.加速蒸发
C.防止液滴飞溅 D.引流缓冲
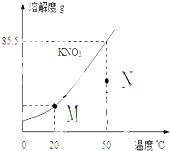
(6)如图为硝酸钾的溶解度曲线.M、N两点分别表示硝酸钾的两种溶液.下列做法能实现M、N间的相互转化的是________
A.从M→N:先将M升温再将其蒸发掉部分水
B.从M→N:先将M升温再将加入适量固体硝酸钾
C.从N→M:先将N降温再加入适量固体硝酸钾
D.从N→M:先过滤出适量固体硝酸钾再降温.
解:(1)40℃时,氯化钠固体的溶解度36.6g;
(2)60℃时硝酸钠的溶解度110g,所以60℃时在100g水中加入100g硝酸钾固体,充分溶解后所形成的溶液是不饱和溶液;
(3)20℃时硝酸钠的溶解度31.6g,所以将上述(2)中溶液降温到20℃时,析出的晶体质量是100g-31.6g=68.4g;
(4)硝酸钾的溶解度受温度影响较大,①析出的晶体中主要物质是硝酸钾(KNO3);②剩余溶液含有氯化钠,又含有硝酸钾,且两者都达到饱和;
(5)20℃时氯化钠固体的溶解度36.0g,所以20℃时,将18克氯化钠溶解在50克水中才能饱和,应至少蒸发30g 水才能形成饱和溶液,蒸发时要用到玻璃棒,其作用是加速蒸发和防止液滴飞溅;
(6)根据溶解度曲线的含义可知从M→N:先将M升温再将加入适量固体硝酸钾.
故答案为:(1)36.6;(2)不饱和;(3)68.4;(4)硝酸钾(KNO3);C;(5)30;B C;(6)B.
分析:(1)根据40℃时,氯化钠固体的溶解度36.6g进行解答;
(2)根据60℃时硝酸钠的溶解度110g进行解答;
(3)根据20℃时硝酸钠的溶解度31.6g进行解答;
(4)根据硝酸钾的溶解度受温度影响较大进行解答;
(5)根据20℃时氯化钠固体的溶解度36.0g进行解答;
(6)根据溶解度曲线的含义进行解答.
点评:本题难度不是很大,主要考查了固体溶解度曲线的作用,根据溶解度曲线可以解决什么问题,从而加深学生对固体溶解度概念的理解,培养学生灵活的运用有关溶解度的知识的能力.
(2)60℃时硝酸钠的溶解度110g,所以60℃时在100g水中加入100g硝酸钾固体,充分溶解后所形成的溶液是不饱和溶液;
(3)20℃时硝酸钠的溶解度31.6g,所以将上述(2)中溶液降温到20℃时,析出的晶体质量是100g-31.6g=68.4g;
(4)硝酸钾的溶解度受温度影响较大,①析出的晶体中主要物质是硝酸钾(KNO3);②剩余溶液含有氯化钠,又含有硝酸钾,且两者都达到饱和;
(5)20℃时氯化钠固体的溶解度36.0g,所以20℃时,将18克氯化钠溶解在50克水中才能饱和,应至少蒸发30g 水才能形成饱和溶液,蒸发时要用到玻璃棒,其作用是加速蒸发和防止液滴飞溅;
(6)根据溶解度曲线的含义可知从M→N:先将M升温再将加入适量固体硝酸钾.
故答案为:(1)36.6;(2)不饱和;(3)68.4;(4)硝酸钾(KNO3);C;(5)30;B C;(6)B.
分析:(1)根据40℃时,氯化钠固体的溶解度36.6g进行解答;
(2)根据60℃时硝酸钠的溶解度110g进行解答;
(3)根据20℃时硝酸钠的溶解度31.6g进行解答;
(4)根据硝酸钾的溶解度受温度影响较大进行解答;
(5)根据20℃时氯化钠固体的溶解度36.0g进行解答;
(6)根据溶解度曲线的含义进行解答.
点评:本题难度不是很大,主要考查了固体溶解度曲线的作用,根据溶解度曲线可以解决什么问题,从而加深学生对固体溶解度概念的理解,培养学生灵活的运用有关溶解度的知识的能力.

练习册系列答案
相关题目
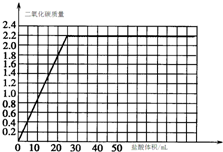
某学生在课外活动中用一定量的二价金属R和稀硫酸反应来制取氢气,所做5次实验结果记录如下表(假设每次实验所产生的氢气全部被收集,体积在同温同压时测定).
根据上述实验结果进行分析、计算,并回答下列问题:
(1)上述实验中,金属一定过量的组的编号是 ,稀硫酸一定过量的组的编号是 .
(2)若在当时实验条件下,氢气的密度为0.085g/L,则反应所用金属R的相对原子质量为 .
(3)若所使用的稀硫酸的密度为1.12g/cm3,则反应所用的硫酸溶液中溶质的质量分数为 .
| 实验编号 | R的质量/g | 稀硫酸的体积/mL | 生成H2的体积/L |
| ① | 1.5 | 50.0 | 1.47 |
| ② | 2.0 | 50.0 | 1.96 |
| ③ | 2.2 | 50.0 | 2.16 |
| ④ | 2.5 | 50.0 | 2.16 |
| ⑤ | 3.0 | 50.0 | 2.16 |
(1)上述实验中,金属一定过量的组的编号是
(2)若在当时实验条件下,氢气的密度为0.085g/L,则反应所用金属R的相对原子质量为
(3)若所使用的稀硫酸的密度为1.12g/cm3,则反应所用的硫酸溶液中溶质的质量分数为
下表是某市城市居民常用的气体燃料、价格和热值,通过分析回答下列问题:
|
燃料 |
价格 |
热值 |
|
煤气 |
1.25元/Kg |
1.56×107/Kg |
|
石油液化气 |
2.50元/Kg |
4.5×107/Kg |
|
天然气 |
1.4元/Kg |
3.9×107/Kg |
(1)从经济角度考虑,选用哪种燃料更适合?________原因是________
(2)实验证明,在同温、同压下,相同体积的任何气体中含有相同的分子数。根据此结论回答下列问题(以下气体均处在同温同压下)
①将同体积的CO(煤气的主要成分)和CH4(天然气的主要成分)混合,所得的混合气体中,碳、氢、氧元素的原子个数比为________,碳、氢元素的质量比为________(化成最简整数比)________
②分别写出CO、CH4燃烧的化学方程式________、________
下表是某市城市居民常用的气体燃料、价格和热值,通过分析回答下列问题:
|
燃料 |
价格 |
热值 |
|
煤气 |
1.25元/Kg |
1.56×107/Kg |
|
石油液化气 |
2.50元/Kg |
4.5×107/Kg |
|
天然气 |
1.4元/Kg |
3.9×107/Kg |
(1)从经济角度考虑,选用哪种燃料更适合?________原因是________
(2)实验证明,在同温、同压下,相同体积的任何气体中含有相同的分子数。根据此结论回答下列问题(以下气体均处在同温同压下)
①将同体积的CO(煤气的主要成分)和CH4(天然气的主要成分)混合,所得的混合气体中,碳、氢、氧元素的原子个数比为________,碳、氢元素的质量比为________(化成最简整数比)________
②分别写出CO、CH4燃烧的化学方程式________、________