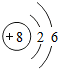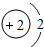题目内容
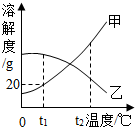 甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( )| A、甲物质的溶解度为20g |
| B、t1℃时,30g甲加入到50g水中可得80g溶液 |
| C、t2℃时,乙物质的饱和溶液升温变成不饱和溶液 |
| D、t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲<乙 |
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小;
B、t1℃时,甲的溶解度是20g;
C、乙物质的溶解度随着温度的升高而减小;
D、饱和溶液的溶质质量分数=
×100%.
B、t1℃时,甲的溶解度是20g;
C、乙物质的溶解度随着温度的升高而减小;
D、饱和溶液的溶质质量分数=
| 溶解度 |
| 100g+溶解度 |
解答:解:A、t1℃时,甲物质的溶解度为20g,其它温度时,甲的溶解度不是20g,该选项说法不正确;
B、t1℃时,30g甲加入到50g水中,只有10g溶解,可得60g溶液,该选项说法不正确;
C、t2℃时,乙物质的饱和溶液升温后,仍然是饱和溶液,该选项说法不正确;
D、t2℃,甲的溶解度大于乙的溶解度,两物质的饱和溶液大小关系是甲>乙,分别降温到t1℃时,甲仍然是饱和溶液,溶解度减小,质量分数也减小,而乙变成不饱和溶液,质量分数不变,因为t2℃时,乙物质的溶解度大于t1℃时甲的溶解度,所以t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是甲<乙,该选项说法正确.
故选:D.
B、t1℃时,30g甲加入到50g水中,只有10g溶解,可得60g溶液,该选项说法不正确;
C、t2℃时,乙物质的饱和溶液升温后,仍然是饱和溶液,该选项说法不正确;
D、t2℃,甲的溶解度大于乙的溶解度,两物质的饱和溶液大小关系是甲>乙,分别降温到t1℃时,甲仍然是饱和溶液,溶解度减小,质量分数也减小,而乙变成不饱和溶液,质量分数不变,因为t2℃时,乙物质的溶解度大于t1℃时甲的溶解度,所以t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是甲<乙,该选项说法正确.
故选:D.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
下列4个图象分别表示对应的四种操作过程,其中正确的是( )
A、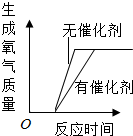 加热氯酸钾制取氧气 |
B、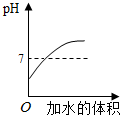 向硫酸溶液不断加水 |
C、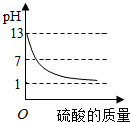 在氢氧化钠溶液中不断滴入硫酸溶液 |
D、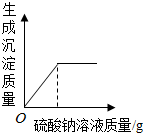 向10.4g10%的BaCl2溶液中逐滴加入10%的 Na2SO4溶液 |
下列实验操作正确的是( )
A、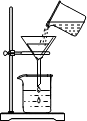 液体过滤 |
B、 取用粉状药品 |
C、 加 加热KMnO4制氧气 |
D、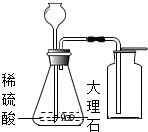 制取CO2 |
许多物质在溶液中都以离子形式存在.我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀的一类化学反应.如:氢氧化钠与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程.结合信息,你认为下列各组离子间不能反应的是( )
| A、H+Na+ OH- N03- |
| B、Na+ K+ Cl- OH- |
| C、H+ K+ CO32-HCO3- |
| D、K+Ba2+Cl-SO42- |
两个或多个同种含氧酸分子之间可以脱水形成相对分子质量更大的酸,如硫酸(H2SO4)可形成H2S3O10或H2S4O13等.下列物质不属于磷酸脱水后形成的是( )
| A、H4P2O7 |
| B、H3P3O9 |
| C、H2P2O7 |
| D、H5P3O10 |
下列物质长时间放置在空气中,质量会增加且变质的是( )
| A、浓盐酸 | B、浓硫酸 |
| C、氧化钙 | D、食盐 |
把过量的铁粉放入Al(NO3)3和AgNO3的混合溶液中,搅拌,待充分反应后过滤,滤纸上留下的是( )
| A、Ag |
| B、Al和Fe |
| C、Ag和Fe |
| D、Ag、Fe和Al |
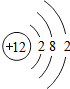
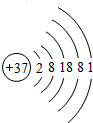
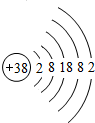 据《自然》杂志报道,科学家最近研制的一种以锶原子做钟摆的钟是世界上最精确的钟.锶元素(元素符号为Sr)原子结构示意图如图所示.下列元素与其处于同一族的是( )
据《自然》杂志报道,科学家最近研制的一种以锶原子做钟摆的钟是世界上最精确的钟.锶元素(元素符号为Sr)原子结构示意图如图所示.下列元素与其处于同一族的是( )