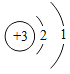题目内容
【题目】某工厂排放的废水中含有亚硫酸钠(Na2SO3) ,若不经处理直接排放,会造成污染。现向50g的废水中加人CaCl2溶液,恰好完全反应,反应后过滤、洗涤、干煤得到固体的质量为6g,试计算: (提示: ![]() ,且废水中的其他杂质不与CaCl2反应)
,且废水中的其他杂质不与CaCl2反应)
(1)亚硫酸钠中钠元素的质量分数__________。(结果保留至0.1%)
(2)废水中亚硫酸钠的质量分数__________。
【答案】36. 5% 12. 6%
【解析】
根据亚硫酸钠的化学式求算钠元素质量分数,根据生成的沉淀质量和对应的化学方程式求算废水中亚硫酸钠质量分数
(1)亚硫酸钠中钠元素质量分数为
![]()
答;亚硫酸钠中钠元素质量分数36.5%
(2)解:设废水中亚硫酸钠的质量为x
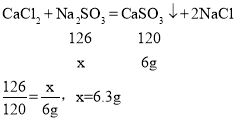
故废水中亚硫酸钠的质量分数;
![]()
答:废水中亚硫酸钠质量分数12.6%

 导学全程练创优训练系列答案
导学全程练创优训练系列答案【题目】钥匙是生活中常用的一种开锁工具,如图是生活中常见的几种钥匙及其材料。
实物图片 |
|
|
|
材料成分 | 不锈钢 | 铁、塑料 | 塑料、铜锌合金 |
(1)所示材料中属于合成材料的是_______________,属于金属材料的是_______________。(填一种即可)
(2)锈蚀的锁,往锁孔里加人一些从铅笔芯上刮下的粉末,有利于锁的开启。这是因为____________。 生活中防止铁生锈的方法很多,请你举出一种常用的防锈方法:______________。
(3)现代生活中广泛用塑料代替钢和其他合金,其原因是______________。 (写一点即可)
(4)为比较锌、铁、铜的活动性顺序,下列方案中选取药品合理的是______________。
A锌、铁、CuSO4溶液
B锌、铜、FeSO4溶液
C锌、CuSO4溶液、FeSO4溶液
D铁、ZnSO4溶液、CuSO4溶液
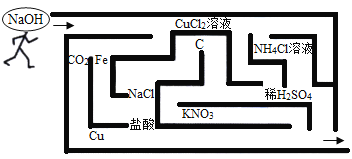
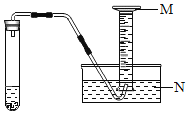
【题目】小明、小红二位同学为探究盐酸的化学性质,做了如下实验:
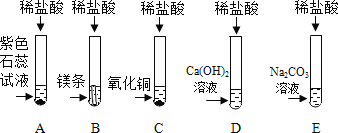
(1)试管 A 中的现象是______。
(2)试管 C 中反应的化学方程式为______。
(3)小明同学把反应后 D、E 试管中的废液倒入一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成。过滤,得到白色沉淀和无色滤液。 小明同学欲探究无色滤液中的溶质成分:小明同学分析得出无色滤液中一定不含 HCl,理由是______。
(提出问题)无色滤液的溶质是什么?
(作出猜想)①NaCl; ②NaCl 和 CaCl2; ③NaCl、CaCl2和 Na2CO3; ④NaCl 和 Na2CO3.小红认为猜想______ 一定不正确。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
①取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想④成立 |
②取少量滤液于试管中,滴加少量 ______ | ______ |