题目内容
【题目】根据装置图回答。
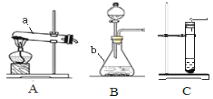
Ⅰ.写出图中仪器a的名称是 ,仪器b的名称 。
Ⅱ.在图中若用无水醋酸钠和碱石灰两种固体药品加热制取甲烷气体,可选用的发生装置是 ;装置B 和C都可以用过氧化氢溶液和二氧化锰制取氧气,写出该反应的化学方程式 ;装置B和C相比,B装置的优点是 。
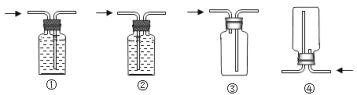
Ⅲ.以下收集装置中能用于收集氧气的是 。
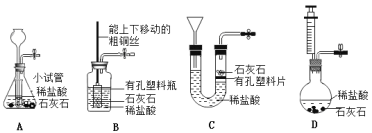
Ⅳ.以下具有启普发生器功能的简易气体发生装置是 。
【答案】Ⅰ 试管,锥形瓶
ⅡA, 2H2O2 ![]() 2H2O+O2↑, 添加液体方便,同时能控制加入液体的速率,使反应能平稳进行
2H2O+O2↑, 添加液体方便,同时能控制加入液体的速率,使反应能平稳进行
Ⅲ.①④ 2
Ⅳ.C
【解析】
试题分析:Ⅱ. 根据反应物的状态和反应条件选择发生装置,用无水醋酸钠和碱石灰两种固体药品加热制取甲烷气体,属固固加热型,选 A装置;用过氧化氢溶液和二氧化锰制取氧气,生成氧气的同时还生成了水:2H2O2![]() 2H2O+O2↑;过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速率和生成氧气的量,故要控制其反应速率,可通过控制过氧化氢的加入量来实现;分液漏斗就可以控制加入液体药品的量和速率;
2H2O+O2↑;过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速率和生成氧气的量,故要控制其反应速率,可通过控制过氧化氢的加入量来实现;分液漏斗就可以控制加入液体药品的量和速率;
Ⅲ、若利用排水法收集氧气,水只能从底部排出,故选①;若是排空气法收集氧气,由于氧气的密度比空气大,会先聚集在集气瓶的底部,故选④;
Ⅳ、启普发生器要符合“随开随用、随关随停”的原则。能节约药品,控制反应的发生和停止,可随时向装置中添加液体药品。故选C。

练习册系列答案
相关题目