题目内容
【题目】学校在进行消防演练过程中,老师带领学生使用干粉灭火器进行模拟灭火演练。化学兴趣小组收集灭火后残留的白色固体,探究其成分。(不考虑杂质的影响)
(查阅资料)
①干粉灭火器的主要成分是NaHCO3;
②![]() ;
;
③碳酸氢钠与氯化钙不发生反应。
请写出干粉灭火器的灭火原理:_____。
(提出猜想)
猜想一:固体成分为Na2CO3;
猜想二:固体成分为NaHCO3;
猜想三:固体成分为_____。
(实验验证)
步骤 | 现象 | 结论 |
小明同学取少量白色固体于试管中,加水溶解,再滴入无色酚酞溶液 | 无色酚酞溶液变红 | 猜想一成立 |
(提出质疑)小红认为小明得出的结论不准确。小红知道NaHCO3在医疗上是治疗胃酸过多症的一种药剂,推测NaHCO3的水溶液可能显_____性,并通过实验得到了验证。
小明和小红继续实验探究:
步骤 | 现象 | 结论 |
1.取少量白色固体加热,将生成的气体通入澄清石灰水中。 | 澄清石灰水变浑浊 | 固体中含有NaHCO3,写出石灰水变浑浊的化学方程式:_____。 |
2.另取少量的白色固体加水溶解,向所得溶液中滴入氯化钙溶液。 | _____ | 固体中含有Na2CO3,写出发生反应的化学方程式:_____。 |
(得出结论)猜想三成立。
(反思交流)师生通过交流又设计了另一种实验方案。
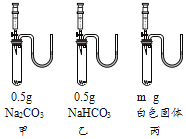
实验装置 | 步骤 | 现象 | 结论 |
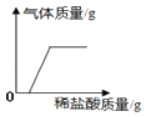
| m的数值为_____g;将注射器内等质量分数的足量稀盐酸同时加入试管中,关闭弹簧夹,观察现象。 | 甲、乙、丙的三支试管中均有气泡产生,U型管右侧液面均升高,待反应结束后液面由高到低的顺序为_____。 | 猜想三成立 |
(拓展延伸)掌握和运用定性和定量分析的方法有利于我们认识化学反应过程,更有助于解决生活、生产实践中的问题。
【答案】碳酸氢钠受热分解得到二氧化碳,因而隔离了空气而灭火 NaHCO3和Na2CO3 碱 Ca(OH)2+CO2=CaCO3↓+H2O 有白色沉淀生成 Na2CO3+CaCl2=CaCO3↓+2NaCl 0.5 乙>丙>甲
【解析】
[查阅资料]
根据干粉灭火器的主要成分是NaHCO3和![]() ,知道干粉灭火器的灭火原理是碳酸氢钠受热分解得到二氧化碳,因而隔离了空气而灭火;
,知道干粉灭火器的灭火原理是碳酸氢钠受热分解得到二氧化碳,因而隔离了空气而灭火;
[提出猜想]
由干粉灭火器的主要成分是NaHCO3和![]() 可知:灭火后残留的白色固体分为三种可能:NaHCO3全部反应、NaHCO3部分反应、NaHCO3没有反应,所以猜想三固体成分为NaHCO3和Na2CO3;
可知:灭火后残留的白色固体分为三种可能:NaHCO3全部反应、NaHCO3部分反应、NaHCO3没有反应,所以猜想三固体成分为NaHCO3和Na2CO3;
[提出质疑]
NaHCO3和Na2CO3的水溶液都显碱性,小明同学取少量白色固体于试管中,加水溶解,再滴入无色酚酞溶液,无色酚酞溶液变红,不能证明猜想一成立;
取少量白色固体加热,将生成的气体通入澄清石灰水中,澄清石灰水变浑浊,是碳酸氢钠在加热条件下反应生成了二氧化碳,二氧化碳使澄清石灰水变浑浊,反应方程式为:
![]() ;
;
另取少量的白色固体加水溶解,向所得溶液中滴入氯化钙溶液,而碳酸氢钠与氯化钙不发生反,如果固体中含有Na2CO3,则碳酸钠和氯化钙溶液反应生成白色沉淀,反应方程式为:
![]() ;
;
[反思交流]
根据控制变量法,本实验中不变量之一是物质的质量,得出m的值为0.5g;
将注射器内等质量分数的足量稀盐酸同时加入试管中,根据反应方程式:
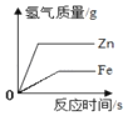
![]() ,相同质量的碳酸钠、碳酸氢钠、碳酸钠和碳酸氢钠的混合物分别与稀盐酸反应,生成二氧化碳的质量是碳酸氢钠反应生成最多,其次是碳酸钠和碳酸氢钠的混合物,最后是碳酸氢钠。所以关闭弹簧夹,甲、乙、丙的三支试管中均有气泡产生,U型管右侧液面均升高,待反应结束后液面由高到低的顺序为乙>丙>甲。
,相同质量的碳酸钠、碳酸氢钠、碳酸钠和碳酸氢钠的混合物分别与稀盐酸反应,生成二氧化碳的质量是碳酸氢钠反应生成最多,其次是碳酸钠和碳酸氢钠的混合物,最后是碳酸氢钠。所以关闭弹簧夹,甲、乙、丙的三支试管中均有气泡产生,U型管右侧液面均升高,待反应结束后液面由高到低的顺序为乙>丙>甲。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】某化学兴趣小组的同学向氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象。
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量。
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告。
同学 | 实验操作 | 现象 | 结论 |
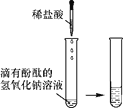
甲 |
| 溶液由红色变成________ | 氢氧化钠与盐酸发生了化学反应,反应的化学方程式为__________ |
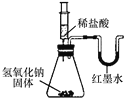
乙 |
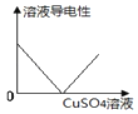
| U形玻璃管中________边的红墨水液面下降(所加稀盐酸的体积忽略不计) | 氢氧化钠与盐酸发生了化学反应 |
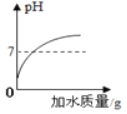
丙 | 用________测定氢氧化钠溶液的pH;向其中滴加足量的稀盐酸后,再测定溶液的pH | 最后溶液的pH________(填“≥7”“≤7”或“不变”) | 氢氧化钠与盐酸发生了化学反应 |
【评价反思】你认为实验设计方案不合理的同学是________,理由是______________________________。