题目内容
【题目】通过一段时间的学习,我们掌握了一些气体的制备方法,例如制取氧气有:
①分离液态空气 ②加热高锰酸钾 ③分解过氧化氢 ④加热分解氯酸钾等等;也熟悉了一些气体的制取和收集装置,例如:

(1)写出上图实验装置中编号仪器的名称:①_____
(2)以上制取氧气的方法中,属于物理方法制氧气的有_____(填序号、下同);属于分解反应的有_____。
(3)若用高锰酸钾制取氧气,发生装置可选用_____(填装置序号).其制取原理用文字表达式表示为_____;若使用E装置收集氧气则验满的方法是_____;实验结束,停止加热时要先把导管移出水面;其理由是_____。
(4)若用分解过氧化氢制取氧气,应选用的的收集装置是_____(填装置序号).其制取原理用文字表达式表示为_____。
(5)实验室用高锰酸钾制取氧气实验主要步骤有①装药品;②检查装置气密性;③加热:④装置固定在铁架台上;⑤熄灭酒精灯;⑥收集气体;⑦将导管移出水槽。实验的正确的操作顺序为_____
A ①②③④⑤⑥⑦ B ②①④③⑥⑤⑦ C ①②④③⑥⑤⑦ D ②①④③⑥⑦⑤
【答案】锥形瓶 ① ②③④ B 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 将带火星的木条,放在集气瓶口,若木条复燃,则氧气集满 防止水倒吸,炸裂试管。 C或E 过氧化氢
锰酸钾+二氧化锰+氧气 将带火星的木条,放在集气瓶口,若木条复燃,则氧气集满 防止水倒吸,炸裂试管。 C或E 过氧化氢![]() 水+氧气 D
水+氧气 D
【解析】
解:(1)据图可知仪器①的名称是锥形瓶;
(2)生成新物质的方法是化学变化,无新物质生成的是物理变化,工业分离液态空气制取氧气无新物质生成,属于物理方法;②加热高锰酸钾、③分解过氧化氢、④加热分解氯酸钾都是分解反应;
(3)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应的文字表达式是:高锰酸钾![]() 锰酸钾+二氧化锰+氧气;该反应需要加热,属于固体加热型,故选发生装置B;用排空气法收集一瓶氧气,验满的方法是:将带火星的木条置于集气瓶口,若木条复燃,说明已经收集满;实验结束后为防止水倒流入试管,引起试管的炸裂,必须先将导管移出水面,后熄灭酒精灯;
锰酸钾+二氧化锰+氧气;该反应需要加热,属于固体加热型,故选发生装置B;用排空气法收集一瓶氧气,验满的方法是:将带火星的木条置于集气瓶口,若木条复燃,说明已经收集满;实验结束后为防止水倒流入试管,引起试管的炸裂,必须先将导管移出水面,后熄灭酒精灯;
(4)氧气不易溶于水且密度比空气大,应选择收集装置C或E;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的文字表达式是:过氧化氢![]() 水+氧气;
水+氧气;
(5)制取氧气时,需要先检验装置气密性,然后装药,固定加热,收集氧气,实验结束先撤导管,后熄灭酒精灯,所以正确的操作顺序为②①④③⑥⑦⑤。

【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:氧化铜[CuO]能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
(猜想)
Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质都不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质都发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后_____。
(实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
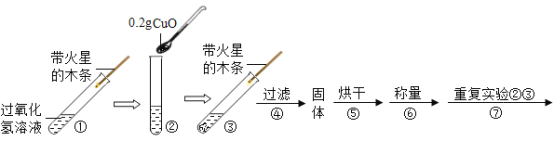
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_____,带火星的木条复燃。 | _____ | 溶液中有气泡放出,_____ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(2)过氧化氢能被CuO催化分解放出O2的反应式为_____。
(实验拓展):
(3)某同学想比较二氧化锰和氧化铜对过氧化氢分解的催化效果,他需要对某些变量进行控制,其中包括有:_____。(至少三点)
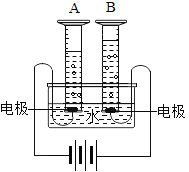
【题目】生活中我们经常发现存放的铁钉会生锈。

(1)小牛和小明通过如图所示实验对铁制品生锈的条件进行探究。通过观察和试管B中加入植物油的目的是___________________。我得出铁生锈的条件是_______________。
(2)在实验室用稀盐酸除铁锈的实验中,小牛认为盐酸中含有H2O、H+、Cl―三种粒子,为了探究稀盐酸中哪种粒子能使铁锈溶解,他进行了如下实验,我能帮他完成。
实验步骤 | 实验现象 | 实验结论 | 设计实验的目的 |
向装有锈铁钉的试管中加入足量NaCl溶液,振荡 | 铁锈不溶解 | _________ | _________ |
小明认为还需要补做一个“向装有锈铁钉的试管中加入水”的对比实验,我认为这个实验是多余的,理由是_____________。小明在做铁钉除锈实验时,由于忘了及时从稀盐酸中取出已除掉铁锈的铁钉,过了一段时间后,他发现铁钉表面居然出现了黑色物质。通过分析我认为铁钉表面的黑色物质可能是_____________。
(3)为了探究铁锈除掉后溶液的组成,小牛将生锈的铁钉放入一支试管中,加入一定量的稀盐酸,待铁钉表面的铁锈恰好溶解完时,迅速取出铁钉,再进行以下实验。
实验步骤 | 实验现象 | 实验结论 |
向取出铁钉的溶液中加入过量的铁粉 | _________ | _________ |
我能写出(3)中的一个化学方程式_________
(4)通过以上探究,我获得的启示是_____________。