��Ŀ����
����Ŀ��������ұ�������ʹ��Դ�õ��˳�����á�
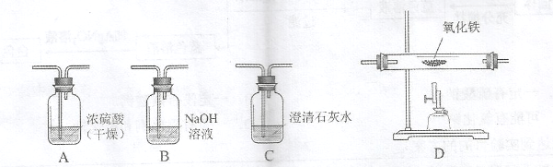
�ٻ�������ԭ����Fe2O3+3CO ![]() 2Fe +3CO2��ʵ�������в�����CO������CO2��ˮ����������Ҫ�ô����������һ����̼��ԭ���������������ɵ����壬����װ�õ���ȷ����˳��Ϊ������ÿ������ȫ��Ӧ��װ�ò����ظ�ʹ������������CO���� 27 �� ������ĸ����
2Fe +3CO2��ʵ�������в�����CO������CO2��ˮ����������Ҫ�ô����������һ����̼��ԭ���������������ɵ����壬����װ�õ���ȷ����˳��Ϊ������ÿ������ȫ��Ӧ��װ�ò����ظ�ʹ������������CO���� 27 �� ������ĸ����
��ʪ����ͭ��ԭ������ϡ���Ὣ��ʯ�е�����ͭ�ܽ⣬Ȼ���ýϻ��õĽ����û���ͭ����0.2mol���۷�����������ͭ��Һ�У���������������28��gͭ�����ݻ�ѧ����ʽ������
�������Ӻ���CuSO4�ķ�Һ�л���ͭ��ͬʱ�õ���ҵԭ�ϡ��������������塣��Ʒ������£�
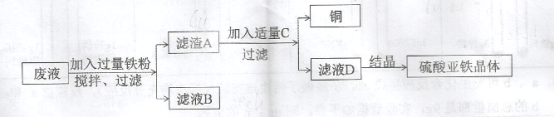
I.����A�ijɷ����� 29�� ��C�������� 30�� ��
II.���������������������ʵĽǶȷ������÷�����һ������֮������ 31�� ��
������ͭ��ұ���ͻ��չ����У�ͭԪ�ش�����̬�ı仯���� 32�� ��
A.����̬������̬ B.����̬������̬
���𰸡���27��BADC ;
��28��12.8;
��29��ͭ������
��30��ϡ���
��31��δ��������B��Һ�е�����������
��32��B
��������
���������ȼ����Ҫ����ʵ�������в�����CO������CO2��ˮ����������Ҫ�ô����������һ����̼��ԭ���������������ɵ����壬�������е�Ҫ��Ҫ�ȳ�ȥ������̼����������������ˮ����������������ʵ�飬����ȷ����˳��ΪBADC ; �ڽ�0.2mol���۷�����������ͭ��Һ�У�������������ͭ������ΪX
Fe+CuSO4==Cu+FeSO4
1mol 1mol
0.2mol X/64
X=12.8g
�������Ӻ���CuSO4�ķ�Һ�л���ͭ�����������ṩ��ʵ�鷽����֪I.����A�ijɷ���ʣ����������ɵ�ͭ����Ϊ��������ת��Ϊ�����������壬���������غ㶨��֪��ҺCϡ���II.���������������������ʵĽǶȷ������÷�����һ������֮����δ��������B��Һ�е��������������ڻ������ý���ͭ�Ĺ����У�����ͭ�ɻ���̬ת��Ϊ����̬��