题目内容
四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数,反应原理为:2Na2S4+O2+2H2O=8S↓+4NaOH.【查阅资料】
①Na2S4受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢(水溶液呈酸性).
②硫代硫酸钠(Na2S2O3)可溶于水,常温下与NaOH溶液不反应.
【实验过程】
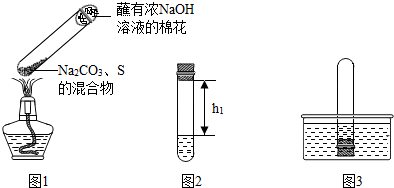
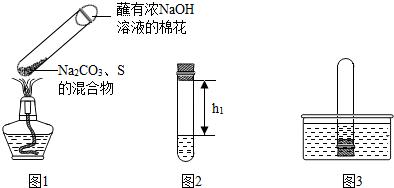
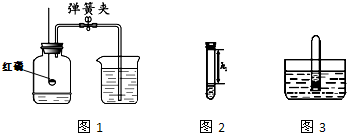
①取0.5g碳酸钠、0.2g硫粉混合后置于试管中,加入(如图1所示,夹持装置已略去),制得Na2S4,反应为:4Na2CO3+12S+X
 2Na2S4+2Na2S2O3+4CO2,X的化学式为______,蘸有浓NaOH溶液的棉花的作用是______.
2Na2S4+2Na2S2O3+4CO2,X的化学式为______,蘸有浓NaOH溶液的棉花的作用是______.
②冷却后,取下棉花,放置一段时间,再向该试管中加入10mL水,迅速塞紧橡胶塞,充分振荡.测量液面至橡胶塞下沿的距离,记录数据h1(如图2所示).
③将该试管插入水中(如图3所示),拔下橡胶塞,观察到______,塞紧橡胶塞.将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2.理论上h2:h1=______.
④按照①~③再重复实验2次.3次实验数据如下表所示.
| 第1次 | 第2次 | 第3次 | |
| h1/cm | 11.0 | 11.4 | 11.6 |
| h2/cm | 8.7 | 9.1 | 9.2 |
【反思与评价】若实验过程②中,取下棉花后,未放置一段时间即进行后续操作,会影响测定结果,请说明有何影响,并阐述理由:______.
③根据四硫化钠和氧气、水反应生成硫和氢氧化钠,会使得试管内压强变小以及空气中氧气约占空气体积的五分之一进行解答;
④【解释与结论】根据空气中氧气的体积分数=
 ×100%进行解答;
×100%进行解答;【反思与评价】根据未放置一段时间会导致试管内的空气成分与外边的空气成分可能有差异进行解答.
解答:解:【实验过程】①根据化学反应前后原子的种类和数目不变和4Na2CO3+12S+X
 2Na2S4+2Na2S2O3+4CO2,可知X的化学式为O2;二氧化碳和NaOH溶液反应生成碳酸钠和水,Na2S4受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢(水溶液呈酸性),所以蘸有浓NaOH溶液的棉花的作用是吸收生成的二氧化碳气体和有毒的硫化氢气体;故填:O2;吸收生成的二氧化碳气体和有毒的硫化氢气体;
2Na2S4+2Na2S2O3+4CO2,可知X的化学式为O2;二氧化碳和NaOH溶液反应生成碳酸钠和水,Na2S4受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢(水溶液呈酸性),所以蘸有浓NaOH溶液的棉花的作用是吸收生成的二氧化碳气体和有毒的硫化氢气体;故填:O2;吸收生成的二氧化碳气体和有毒的硫化氢气体;③四硫化钠和氧气、水反应生成硫和氢氧化钠,会使得试管内压强变小,将该试管插入水中(如图3所示),拔下橡胶塞,观察到水进入试管内,进入水的体积约为试管内空气体积的五分之一;空气中氧气约占空气体积的五分之一,将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2.理论上h2:h1=4:5;故填:水进入试管内,进入水的体积约为试管内空气体积的五分之一;4:5;
④【解释与结论】空气中氧气的体积分数=
 ×100%=20.9%;故填:20.9;
×100%=20.9%;故填:20.9;【反思与评价】未放置一段时间会导致试管内的空气成分与外边的空气成分可能有差异.故填:试管内的空气成分与外边的空气成分可能有差异.
点评:本题考查了二氧化碳、碳酸钠的化学性质及有关测定空气中氧气的体积分数及注重考查学生的分析能力和基本计算能力.

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数,反应原理为:2 Na2S4 + O2 + 2H2O = 8S↓+ 4 NaOH。
【实验资料】
①四硫化钠(Na2S4)的相对分子质量为 ,其中硫元素的质量分数为 (结果精确到0.1%)。
②四硫化钠受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢。
③NaOH溶液呈碱性,可吸收硫化氢、二氧化碳、二氧化硫等酸性气体
④硫代硫酸钠(Na2S2O3)可溶于水,常温下与NaOH溶液不反应。
【实验过程】
①取碳酸钠、 硫粉混合后置于试管中,加热(如图1所示,夹持装置已略去),制得Na2S4,反应为4Na2CO3 + 12S + X  2 Na2S4+ 2 Na2S2O3 + 4CO2,X 的化学式为 ,蘸有浓NaOH 溶液的棉花的作用是 。
2 Na2S4+ 2 Na2S2O3 + 4CO2,X 的化学式为 ,蘸有浓NaOH 溶液的棉花的作用是 。 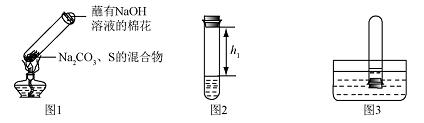
②冷却后,取下棉花,放置一段时间,再向该试管中加入10ml水,迅速塞紧橡胶塞,充分振荡,测量液面至橡胶塞下沿的距离,记录数据h1(如图2所示)
③将该试管插入水中(如图3所求),取下橡胶塞,观察到
,塞紧橡胶塞。将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据h2,理论上h1:h2=
④按照①~③再重复实验2次.3次实验数据如下表所示。
| 第1次 | 第2次 | 第3次 | |
| h1/cm | 11.2 | 11.4 | 11.6 |
| h2/cm | 8.9 | 9.1 | 9.2 |
【解释与结论】根据第1次实验数据,计算空气中氧气的体积分数为 (结果精确到0.1%)。
【反思与评价】(1)若实验过程②中,取下棉花后,未放置一段时间即进行后续操作,会影响测定结果,请说明有何影响,并阐述理由: 。(2分)
(2)若要保证实验的效果,至少需要生成四硫化钠(Na2S4)0.174g ,则理论上实验时至少取碳酸钠粉末 克?
写出计算过程(2分)