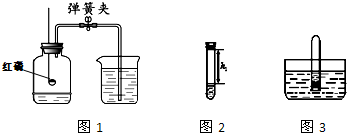
��Ŀ����
��ʵ�����ϡ�
�������ƣ�Na2S4������Է�������Ϊ
������������ʱ����������е�ˮ������Ӧ�����������ж��������⣮
��NaOH��Һ�ʼ��ԣ����������⡢������̼����������������������������ƣ�Na2S2O3��������ˮ����������NaOH��Һ����Ӧ��
��ʵ����̡�
��ȡ̼���ơ���ۻ�Ϻ������Թ��У����ȣ���ͼ1��ʾ���г�װ������ȥ�����Ƶ�Na2S4����ӦΪ4Na2CO3+12S+X
| ||
����ȴ��ȡ����������һ��ʱ�䣬������Թ��м���10mlˮ��Ѹ���������������������Һ�����������صľ��룬��¼����h1����ͼ2��ʾ��
�۽����Թܲ���ˮ�У���ͼ3����ȡ���������۲쵽
�ܰ��բ١������ظ�ʵ��2�Σ�3��ʵ���������±���ʾ��
| ��1�� | ��2�� | ��3�� | |
| h1/cm | 11.2 | 11.4 | 11.6 |
| h2/cm | 8.9 | 9.1 | 9.2 |
����˼�����ۡ���1����ʵ����̢��У�ȡ������δ����һ��ʱ�伴���к�����������Ӱ��ⶨ�������˵���к�Ӱ�죬���������ɣ�
��2����Ҫ��֤ʵ���Ч����������Ҫ���������ƣ�Na2S4��0.174g����������ʵ��ʱ����ȡ̼���Ʒ�ĩ
��ʵ����̡��ٸ��ݻ�ѧ��Ӧǰ��ԭ�ӵ��������Ŀ���䡢������̼��NaOH��Һ��Ӧ�Լ�Na2S4����ʱ����������е�ˮ������Ӧ�����������ж��������⣨ˮ��Һ�����ԣ����н��
�۸��������ƺ�������ˮ��Ӧ��������������ƣ���ʹ���Թ���ѹǿ��С�Լ�����������Լռ������������֮һ���н��
����������ۡ����ݿ������������������=
| h1-h2 |
| h1 |
����˼�����ۡ���1������δ����һ��ʱ��ᵼ���Թ��ڵĿ����ɷ�����ߵĿ����ɷֿ����в�����н��
��2�����������Ƶ�������Ϸ�Ӧ�Ļ�ѧ����ʽ���Լ����̼���Ƶ�������
| 32��4 |
| 174 |
��ʵ����̡��ٸ��ݻ�ѧ��Ӧǰ��ԭ�ӵ��������Ŀ�����4Na2CO3+12S+X
| ||
�������ƺ�������ˮ��Ӧ��������������ƣ���ʹ���Թ���ѹǿ��С�������Թܲ���ˮ�У���ͼ3��ʾ���������������۲쵽ˮ�����Թ��ڣ�����ˮ�����ԼΪ�Թ��ڿ�����������֮һ������������Լռ������������֮һ�����Թ�ȡ������ת����������Һ�����������صľ��룬��¼����h2������֪��������h1��h2=5��4��
����������ۡ��������������������=
| 11.2-8.9 |
| 11.2 |
����˼�����ۡ���1��δ����һ��ʱ��ᵼ���Թ��ڵĿ����ɷ�����ߵĿ����ɷֿ����в��죮����Թ��ڵĿ����ɷ�����ߵĿ����ɷֿ����в��죮
��2������Ҫ̼���Ƶ�����Ϊx
4Na2CO3+12S+O2
| ||
424 348
x 0.174g
| 424 |
| x |
| 348 |
| 0.174g |
��ã�x=0.212g
��������ʵ��ʱ����ȡ̼���Ʒ�ĩ0.212g��
�ʴ�Ϊ����ʵ�����ϡ�174��73.6%��
��ʵ����̡�O2�����ն�����̼��Na2S4���Ȳ������ж��������⣻
�е���ɫ����������Թ���Һ��������5��4��
����������ۡ�20.5%��
����˼�����ۡ���1����δ����һ��ʱ�䣬�����ƫС����Ϊ��һ����Ӧ�������Թܿ����е��������������õڶ�����Ӧ����������ƫ�ͣ��������ƫС��
��2��0.212��

 ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д������ƣ�Na2S4�������������ײⶨ�����������������������Ӧԭ��Ϊ��2 Na2S4 + O2 + 2H2O = 8S��+ 4 NaOH��
��ʵ�����ϡ�
�������ƣ�Na2S4������Է�������Ϊ ��������Ԫ�ص���������Ϊ �������ȷ��0.1%����
������������ʱ����������е�ˮ������Ӧ�����������ж��������⡣
��NaOH��Һ�ʼ��ԣ����������⡢������̼�������������������
����������ƣ�Na2S2O3��������ˮ����������NaOH��Һ����Ӧ��
��ʵ����̡�
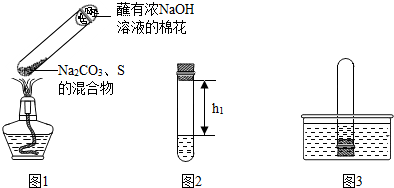
��ȡ̼���ơ� ��ۻ�Ϻ������Թ��У����ȣ���ͼ1��ʾ���г�װ������ȥ�����Ƶ�Na2S4����ӦΪ4Na2CO3 + 12S + X  2 Na2S4+ 2 Na2S2O3 + 4CO2��X �Ļ�ѧʽΪ ��պ��ŨNaOH ��Һ������������ ��
2 Na2S4+ 2 Na2S2O3 + 4CO2��X �Ļ�ѧʽΪ ��պ��ŨNaOH ��Һ������������ �� 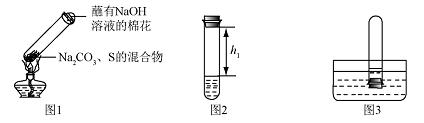
����ȴ��ȡ����������һ��ʱ�䣬������Թ��м���10mlˮ��Ѹ���������������������Һ�����������صľ��룬��¼����h1����ͼ2��ʾ��
�۽����Թܲ���ˮ�У���ͼ3����ȡ���������۲쵽
���������������Թ�ȡ����������������Һ�����������صľ��룬��¼����h2��������h1:h2��
�ܰ��բ١������ظ�ʵ��2�Σ�3��ʵ���������±���ʾ��
| ��1�� | ��2�� | ��3�� | |
| h1/cm | 11.2 | 11.4 | 11.6 |
| h2/cm | 8.9 | 9.1 | 9.2 |
����������ۡ����ݵ�1��ʵ�����ݣ�����������������������Ϊ �������ȷ��0.1%����
����˼�����ۡ�(1)��ʵ����̢��У�ȡ������δ����һ��ʱ�伴���к�����������Ӱ��ⶨ�������˵���к�Ӱ�죬���������ɣ� ����2�֣�
��2����Ҫ��֤ʵ���Ч����������Ҫ���������ƣ�Na2S4��0.174g ,��������ʵ��ʱ����ȡ̼���Ʒ�ĩ �ˣ�
д��������̣�2�֣�
���������ϡ�
��Na2S4����ʱ����������е�ˮ������Ӧ�����������ж��������⣨ˮ��Һ�����ԣ���
����������ƣ�Na2S2O3��������ˮ����������NaOH��Һ����Ӧ��
��ʵ����̡�
��ȡ0.5g̼���ơ�0.2g��ۻ�Ϻ������Թ��У����루��ͼ1��ʾ���г�װ������ȥ�����Ƶ�Na2S4����ӦΪ��4Na2CO3+12S+X
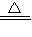 2Na2S4+2Na2S2O3+4CO2��X�Ļ�ѧʽΪ______��պ��ŨNaOH��Һ������������______��
2Na2S4+2Na2S2O3+4CO2��X�Ļ�ѧʽΪ______��պ��ŨNaOH��Һ������������______��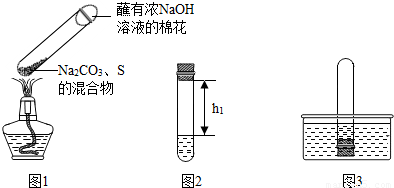
����ȴ��ȡ����������һ��ʱ�䣬������Թ��м���10mLˮ��Ѹ���������������������Һ�����������صľ��룬��¼����h1����ͼ2��ʾ����
�۽����Թܲ���ˮ�У���ͼ3��ʾ���������������۲쵽______���������������Թ�ȡ������ת����������Һ�����������صľ��룬��¼����h2��������h2��h1=______��
�ܰ��բ١������ظ�ʵ��2�Σ�3��ʵ���������±���ʾ��
| ��1�� | ��2�� | ��3�� | |
| h1/cm | 11.0 | 11.4 | 11.6 |
| h2/cm | 8.7 | 9.1 | 9.2 |
����˼�����ۡ���ʵ����̢��У�ȡ������δ����һ��ʱ�伴���к�����������Ӱ��ⶨ�������˵���к�Ӱ�죬���������ɣ�______��