题目内容
【题目】根据下列装置图,回答问题:
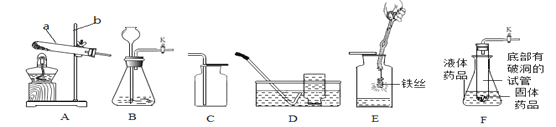
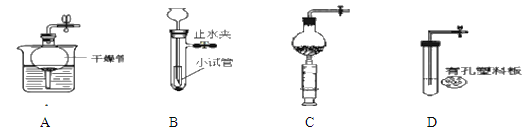
(1)上图中仪器a 的名称是________,仪器b的名称是________。
(2)用高锰酸钾制取氧气的化学反应方程式是_______________,选用的发生装置是____(填序号),为防止高锰酸钾粉末进入导管,该装置需做一点改进的是_____,若用D装置收集氧气,当观察到________时,便可开始收集.
(3)小王同学用高锰酸钾制取收集了一瓶氧气后,测得氧气纯度明显偏低,原因可能是____
A 高锰酸钾中混入了二氧化锰 B 收集前,集气瓶中未注满水
C 收集后,集气瓶中仍有少量水 D 未见气泡连续均匀冒出时就开始收集
(4)利用装置B证明SO2易溶于水,锥形瓶内装满SO2,从长颈漏斗向锥形瓶内注水至如图位置,关闭活塞K,一段时间后可观察到的现象是___________________。(填字母)
A 长颈漏斗中上升一段水柱 B 长颈漏斗下端有气泡冒出
(5)实验室制取二氧化碳选用发生和收集装置的组合是_____(填序号),反应的化学方程式是______________,图F是某同学利用报废试管设计的制二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点________,找出与其有相同优点的装置______
(6)用收集的氧气完成图E铁丝燃烧的实验,集气瓶中预先放少量水的原因是_________。
【答案】试管 铁架台 2KMnO4 ![]() K2MnO4+MnO2+O2↑ A 试管口放棉花 导管口有气泡连续均匀冒出 BD B BC CaCO3 + 2 HCl = CaCl2 + H2O + CO2↑ 控制反应的发生和停止 AC 防止高温生成物溅落炸裂集气瓶底
K2MnO4+MnO2+O2↑ A 试管口放棉花 导管口有气泡连续均匀冒出 BD B BC CaCO3 + 2 HCl = CaCl2 + H2O + CO2↑ 控制反应的发生和停止 AC 防止高温生成物溅落炸裂集气瓶底
【解析】
(1)据图可知,仪器a 的名称是试管,故填试管;
仪器b的名称是铁架台,故填铁架台。
(2)高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,故反应的化学方程式写为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
用高锰酸钾制取氧气的反应物是固体,反应条件是加热,应选择固体受热发生装置,即A,故填A;
用高锰酸钾制取氧气时,为防止高锰酸钾粉末进入导管,应在试管口放棉花,故填试管口放棉花;
D装置为排水法收集气体,刚排出的气体主要为原锥形瓶中的空气,不能收集,当观察到导管口有气泡连续均匀冒出时开始收集气体,故填导管口有气泡连续均匀冒出。
(3)A 二氧化锰是反应的生成物,不会影响氧气的纯度,选项错误;
B 收集前,集气瓶中未注满水,与收集的氧气混合,降低了氧气的纯度,选项正确;
C 收集后,集气瓶中剩余的少量水不会影响氧气的纯度,选项错误;
D 刚排出的气体主要为原锥形瓶中的空气,未见气泡连续均匀冒出时就开始收集,与收集的氧气混合,降低了氧气的纯度,选项正确,故填BD。
(4)锥形瓶内装满SO2,从长颈漏斗向锥形瓶内注水至如图位置,关闭活塞K,如果SO2易溶于水,则锥形瓶内的压强就会变小,且低于瓶外大气压,瓶外的气体会通过长颈漏斗进入锥形瓶,一段时间后可观察到的现象长颈漏斗下端有气泡冒出,故填B。
(5)实验室用石灰石与稀盐酸制取二氧化碳,反应物是固体与液体,不需要加热,应选择固液常温发生装置,即B,二氧化碳能溶于水,且密度比空气的密度大,所以收集二氧化碳只能用向上排空气法,故填BC;
石灰石中的碳酸钙与元素反应生成氯化钙、水和二氧化碳,故反应的化学方程式写为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
F装置可以通过开闭开关K来控制反应的发生与停止,故填可以控制反应的发生与停止;
A 关闭开关,反应生成的被封闭的气体产生较大压强,使干燥管中的液面下降,直至与固体分离,选项正确;
B 小试管仅起到密封长颈漏斗管口的作用,无法使液体与固体分离,关闭止水夹会导致反应生成的气体产生较大的压强将单孔塞弹出,选项错误;
C 关闭开关,反应生成的气体产生较大的压强,使注射器的活塞向外弹出,直至液面与固体分离,选项正确;
D 关闭开关,不能使液体与固体分离,且反应生成的气体产生较大的压强会将弹孔塞弹出,选项错误,故填AC。
(6)铁丝在氧气中燃烧生成的熔融物直接落到集气瓶底部会使瓶底受热不匀发生炸裂,集气瓶中预先放少量水能够防止高温生成物溅落炸裂集气瓶底,故填防止高温生成物溅落炸裂集气瓶底。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案【题目】下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
(1)两种物质中,溶解度受温度影响变化较大的是______(填化学式)。
(2)60℃时,按图示操作:

A中溶质是_______(填“饱和”或“不饱和”)溶液,C中溶液的总质量是________g。
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液________(填“大于”“等于”或“小于”) KNO3溶液。
(4)由表中数据可知,若KNO3和NaCl在T℃时具有相同的溶解度Xg,则X最小的取值范围是____(用数学表达式表示,下同),T最小的取值范围是______