题目内容
【题目】在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的工业流程如图所示。
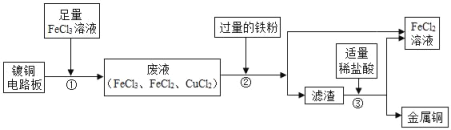
(1)依据流程写出步骤①中Cu和FeCl3反应的化学方程式:_____。步骤②加入铁粉后发生的置换反应的化学方程式为_____。
(2)步骤②得到滤渣的成分是_____;步骤③的操作是_____。
【答案】Cu+2FeCl3═2FeCl2+CuCl2 Fe+CuCl2═FeCl2+Cu Fe和Cu(或铁和铜) 过滤
【解析】
(1)从流程图可以看出,步骤①中Cu和FeCl3反应生成了氯化铜和氯化亚铁,对应的化学方程式:Cu+2FeCl3═2FeCl2+CuCl2.步骤②加入铁粉后发生的置换反应是铁和氯化铜反应生成氯化亚铁和铜,对应的化学方程式为 Fe+CuCl2═FeCl2+Cu。故填:Cu+2FeCl3═2FeCl2+CuCl2; Fe+CuCl2═FeCl2+Cu
(2)步骤②中加入了过量的铁粉,所以得到滤渣的成分是剩余的Fe和生成的Cu(或铁和铜);步骤③实现了固体和液体的分离,实验室中该操作是过滤。故填:Fe和Cu(或铁和铜); 过滤。

【题目】如表列出的是生活和工业中常用的三种漂白剂.
种类 | 亚氯酸钠 | 二氧化氯 | 漂白粉 |
化学式 | NaClO2 | ClO2 | Ca(ClO)2和CaCl2 |
(1)三种漂白剂中,Ca(ClO)2属于___(填序号).
①混合物 ②化合物 ③氧化物
(2)ClO2中氯元素的化合价为___.
(3)表格中的物质(除CaCl2),氧元素的质量分数最大的是___.
(4)次氯酸钙[Ca(ClO)2]是漂白粉的有效成分.
①次氯酸钙在潮湿的空气中久置会生成具有漂白性的物质次氯酸(HClO)和难溶于水的白色固体,反应的化学方程式___,该反应的基本类型是___.
②工业使用漂白粉时常根据(4)中①的反应原理,通过添加少量的___(填序号)物质来解决漂白粉漂白缓慢的问题.
A 氢氧化钠 B 稀盐酸 C 氢氧化钙 D 氯化钠.
【题目】日常生活中,人们利用碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好。下面实验是影响碳酸钠溶液碱性的因素展开探究。用碳酸钠固体和不同温度的水,配置溶质质量分数分别为 2%、6%和10%的碳酸钠溶液,立即测量溶液的pH,记录如下表:
实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
水的温度/°C | 20 | 40 | 60 | 20 | 40 | 60 | 20 | 40 | 60 |
溶液 pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
(1)去油污的效果最好的是___________ (填实验编号)。
(2) 在一定温度范围内,温度对碳酸钠溶液pH的影响是:当_______相同时,______。
(3)如果某实验小组想得到更好的去污效果,根据之前的实验规律,可以尝试的实验条件是__________________
A 12%、 60°C B 8%、 40° C C 10%、 70°C
(4)碳酸钠溶液呈碱性的原因是:一部分碳酸根离子水解产生碳酸氢根离子和氢氧根离子,少部分碳酸氢根离子水解产生碳酸和氢氧根离子。计算100g10%碳酸钠溶液中碳元素的质量是_________g(精确到0.1)