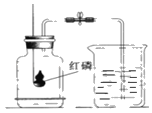
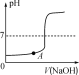
��Ŀ����
����Ŀ�������������������������ȡʵ�飬�����Ҫ����ա����г�������ʡ�ԣ�
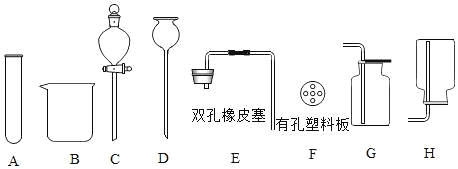
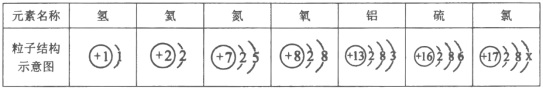
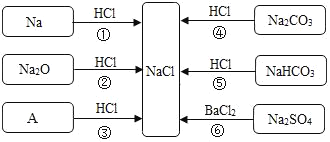
��1�����A������������_____��
��2���ù���������Һ�Ͷ��������������ķ������ռ�װ��Ӧѡ_____����������ţ���ϣ���Ӧ�Ļ�ѧ����ʽ��_____��
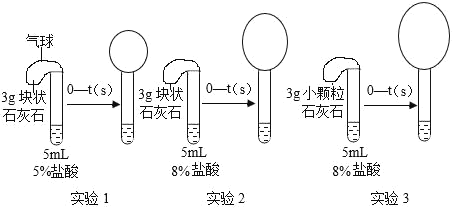
��3����ADEF��װ�ķ���װ��_____����ܡ����ܡ�������ʵ�����ƶ�����̼����װ��_____����ܡ����ܡ����ﵽ��ʱ��ʹ��Ӧ������ֹͣ��Ŀ�ġ�
��4��12.5g��̼���80%�Ĵ���ʯ�����������ᷴӦ���������ɶ�����̼�����ʵ��������ݻ�ѧ����ʽ���㣩_____��
���𰸡��Թ� ACEG��ADEG 2H2O2 ![]() 2H2O+O2�� �� ���� 0.1mol
2H2O+O2�� �� ���� 0.1mol
��������
��1�����A�������������Թܡ�
��2���ù���������Һ�Ͷ���������������Һ������ڳ����·�Ӧ��ȡ���壬���������ܶȴ��ڿ����������������ſ������ռ������Զ�Ӧ�ķ������ռ�װ��ӦѡACEG��ADEG��ϣ���Ӧ�Ļ�ѧ����ʽ�� 2H2O2 ![]() 2H2O+O2����
2H2O+O2����
��3����ADEF��װ�ķ���װ���ǹ����Һ�峣������ȡ����װ�ã�����������ʵ�����ƶ�����̼�����Ǹ�װ����û��ֹˮ�У����Ը�װ�ò��ܴﵽ��ʱ��ʹ��Ӧ������ֹͣ��Ŀ�ġ�
��4���⣺12.5g��̼���80%�Ĵ���ʯ�����������ᷴӦ�������ɶ�����̼�����ʵ���Ϊx
CaCO3+2HCl�TCaCl2+H2O+CO2��
![]()
![]() ����x=0.1mol
����x=0.1mol
�����ɶ�����̼�����ʵ���Ϊ0.1mol��

����Ŀ��MgSO47H2O��һ����Ҫ�Ļ���ԭ�ϣ�ij������һ��þ��ʯ����Ҫ�ɷ�ΪSiO2��MgCO3������������FeCO3�������ɷֺ��ԣ�Ϊԭ���Ʊ�MgSO47H2O����Ҫ������ͼ��
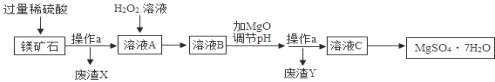
�������ϣ���SiO2�Ȳ�����ˮҲ������ϡ���ᡣ
�ڲ���������������������ʽ����ʱ��Һ��pH���±���
������ | Mg2+ | Fe2+ | Fe3+ |
��ʼ����ʱ��pH | 9.1 | 7.6 | 1.9 |
������ȫʱ��pH | 11.1 | 9.7 | 3.2 |
��ش��������⣺
��1��MgCO3����ϡ����Ļ�ѧ����ʽΪ_____��
��2��Ϊ����þ��ʯ��ϡ�����ַ�Ӧ�����ԭ�������ʣ��ɲ�ȡ�Ĵ�ʩΪ_____������ĸ����
A ��þ��ʯ���� B ���ͷ�Ӧ�¶� C ��ϡ�����ν���
��3������ҺA���м���H2O2��Һ������Fe2��SO4��3���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
��4��ѡ��MgO����pHʹFe3+ת��Ϊ����������ѡ��NaOH��ԭ����_____��
��5��������þ���ں���Һ��pH��Χ��_____���ò���ʽ��ʾ����