题目内容
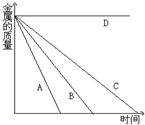
室温下,铁、铜、锌、镁四种金属分别放入相同质量分数的稀盐酸中,如图表示金属质量有酸中减少的情况与时间的关系,写出四条曲线所表示的元素的元素符号:
A______;B______;C______;D______.
A______;B______;C______;D______.

在金属活动顺序表中氢前边的金属可以与稀盐酸反应,但氢以后的金属不会与稀盐酸反应,位置越靠前的金属与酸反应的越剧烈,速度越快,铜排在氢的后面,故铜不与酸反应,图中D的质量一直不变,故为铜,ABC三条线质量减少的快慢分别是A>B>C,故ABC分别为Mg、Zn、Fe.
故答案为:Mg、Zn、Fe、Cu
故答案为:Mg、Zn、Fe、Cu

练习册系列答案
相关题目
