题目内容
【题目】根据要求回答问题.
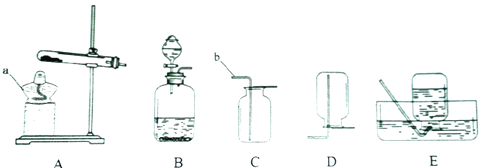
①写出仪器名称:a ;b ;
②用氯酸钾和二氧化锰的混合物制取氧气可选择的装置组合是 (填字母);
③要制取0.03mol氧气,需分解的氯酸钾的物质的量为 ;(根据化学方程式列式计算)
④现从废旧干电池中回收上述实验所需的MnO2.废旧干电池中主要含有C和MnO2(均难溶于水)、ZnCl2和NH4Cl(均易溶于水).为获得较纯的MnO2进行如下实验:
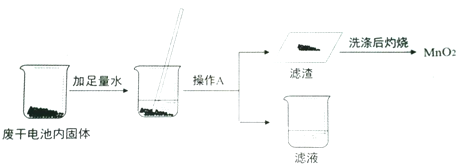
上述实验过程中,加水后用玻璃棒搅拌的作用是 ;操作A的名称是 ;最后“灼烧”的目的是 .
【答案】①酒精灯;导管;
②AC(或AE);
③设需分解的氯酸钾的物质的量为x
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
2 3
x 0.03mol
![]() =
=![]()
x=0.02mol
答:需分解的氯酸钾的物质的量为0.02mol;
④加速溶解;过滤;除去滤渣中混有的C.
【解析】
①标号仪器分别是酒精灯和导管;
②加热氯酸钾和二氧化锰的混合物属于固体加热型,故选发生装置A,氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集;
③设需分解的氯酸钾的物质的量为x
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
2 3
x 0.03mol
![]() =
=![]()
x=0.02mol
答:需分解的氯酸钾的物质的量为0.02mol;
④根据题意,该实验的目的是回收MnO2,故需除去其他物质;
ZnCl2、NH4Cl均易溶于水,所以先将混合物溶于水,溶解操作中,玻璃棒的作用是加速溶解,然后进行过滤,除去可溶性的ZnCl2、NH4Cl,得到碳和二氧化锰的混合物;
C具有可燃性,故步骤c灼烧残渣的目的是除去C,得到纯净的二氧化锰;

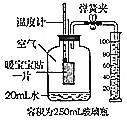
【题目】合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要。
(1)2015年10月22日江西南昌一大型超市发生严重火灾。从燃烧条件分析,超市库房内存放的大量鞋、纸箱等物品充当了 。
(2)高层建筑物通常设计了灭火用的洒水系统。从灭火原理分析,洒水的作用主要是 。
(3)分析下表中的数据,回答问题:
物质代号 | L | M | N | P |
熔点/℃ | -117 | 3550 | 44 | -259 |
沸点/℃ | 78 | 4827 | 257 | -253 |
着火点/℃ | 510 | 370 | 40 | 580 |
①有人认为“物质的熔、沸点越高,着火点越高”,该结论 (填“合理”或“不合理”)。
②已知酒精灯火焰的温度约为500℃。利用如图装置,验证达到可燃物着火点是燃烧的条件之一,上表中可用于完成该实验的两种可燃物是________和________(填代号)。
(4)依据下图进行实验(夹持仪器略去)。实验过程:①通入N2,点燃酒精灯,一段时间后,a、b中均无明显现象;②熄灭酒精灯,立即改通O2,a中无明显现象,b中红磷燃烧。
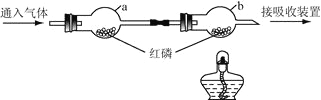
Ⅰ.实验过程②中,红磷燃烧的化学方程式为 。
Ⅱ.实验过程②中,对比a、b中的实验现象,可知可燃物燃烧的条件之一是 。
Ⅲ.实验过程中,能说明可燃物燃烧需要氧气的实验是 。
【题目】工业上用如下工艺流程获得较纯净细白的碳酸钙用作食品添加剂,(石灰石中的杂质高温不分解、不溶于水且不与盐酸反应;氢氧化钙与盐酸反应没有气泡产生)试回答:
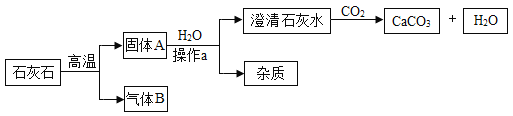
①石灰石高温分解的化学方程式是____________。
②为了节约成本,该工艺中可循环使用的物质是____________。
③有同学对流程中固体A的成分进行实验探究。
I.提出问题:石灰石中的碳酸钙是否完全分解了?
Ⅱ.进行猜想:①碳酸钙全部分解:②____________;③碳酸钙没有分解。
Ⅲ.设计实验方案、进行实验:
下表是对猜想①进行实验探究的过程:
实验步骤 | 实验现象 | 实验结论 |
取样,加适量水溶解,静置取少量上层清液于试管中,滴入酚酞试液;取少量下层固体于试管中,加入足量盐酸。 | 试液变为红色____________ | 碳酸钙全部分解 |
请你对猜想②进行探究,完成下表:
实验步骤 | 实验现象 | 实验结论 |
取样,加适量水溶解,静置,取少量上层清液于试管中,滴入酚酞试液;取少量下层固体于试管中,加入足量盐酸。 | ____________ | ____________ |