题目内容
【题目】利用能源、节约能源、保护环境是我们大家共同关注的问题。

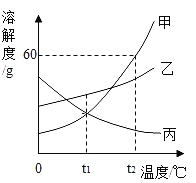
(1)充分燃烧1000 g天然气和煤所产生的CO2和SO2气体的质量如图所示,则_______燃烧对环境影响较小,1000 g煤中硫元素的质量为_______(假设硫元素完全转化为SO2)。
(2)SO2的大量排放能形成酸雨,pH_______(填“<”“>”或“=”)5.6的降雨称为酸雨。在煤燃烧后将烟气通入吸收塔并“喷淋”石灰水进行“脱硫”可减少SO2的排放,石灰水需要“喷淋”的目的是__________。工业上常用熟石灰处理含有硫酸的废水,反应的化学方程式为________________。
(3)目前,在汽车尾气系统中安装催化转化器可将污染物CO、NO转化为无毒的CO2和N2,化学方程式为:_______________。请根据“在化学反应过程中有元素化合价变化的化学变化,叫做氧化还原反应”判断,该反应_______(填“是”或“不是”)氧化还原反应。
【答案】天然气 5g < 使SO2被充分吸收 H2SO4+Ca(OH)2=CaSO4+2H2O 2CO+2NO 2CO2+N2 是
2CO2+N2 是
【解析】
解:(1)两种燃料燃烧对环境影响较小的是天然气;由图可知1000g煤产生10g二氧化硫,其中硫元素的质量为10g×![]() ×100%=5g;
×100%=5g;
(2)SO2的大量排放能形成酸雨,其pH<5.6;根据题意,H2SO4和石灰水反应生成硫酸钙和水,反应的化学方程式为H2SO4 +Ca(OH)2 ═CaSO4+2H2O;
(3)一氧化碳与一氧化氮在催化剂的作用下反应生成二氧化碳与氮气,凡有元素化合价变化的化学反应就叫做氧化还原反应,反应前后,氮元素的化合价发生了改变,则该反应属于氧化还原反应。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(实验探究)
实验步骤 | 实验现象 |
Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
(实验结论)
(1)A中产生的气体是_____________。
(2)实验Ⅱ、Ⅲ证明:氧化铁的___________和____________在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂。
(3)写出氧化铁催化过氧化氢溶液分解的化学方程式 ____________。
(实验评价)
(1)实验设计Ⅳ的目的是比较__________________。
(实验拓展)
(1)查阅资料得知:CuO、CuSO4、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是______________(填序号)。
A MnO2只能作过氧化氢溶液分解的催化剂
B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率
D 用作催化剂的物质不可能是其他反应的反应物或生成物