题目内容
【题目】小杰在做铁丝在纯氧中燃烧的实验时,发现燃烧产物是一种不溶于水的黑色固体,小杰想进一步探究该黑色固体的成分。
(1)在做铁丝燃烧实验时,除了生成黑色固体外还观察到的现象是:_________。
(2)对黑色固体的探究:
(查阅资料)
① FeO 和 Fe3O4 都是黑色固体,而且都可和稀盐酸或稀硫酸反应。其中 Fe3O4 和稀硫酸反应生成铁盐、亚铁盐和水,请你写出该反应的化学方程式:________。
② KSCN 溶液遇铁离子显血红色。
(猜 想)
猜想a. 该黑色固体不是Fe2O3, 因为___________________;
猜想b. 该黑色固体是___;
猜想c. 该黑色固体是Fe3O4;
猜想d. 该黑色固体是 FeO 和 Fe3O4 的混合物。
(实验设想)向黑色固体加入过量稀硫酸的实验过程中,
如果猜想b 成立,则反应后溶液中所含的金属离子为______(写化学符号);
如果猜想c 成立,则反应后溶液中所含的溶质有_____(写化学式)。
(实验方案)
方案一:取上述固体于烧杯中,加入适量的稀硫酸,过滤后向滤液中滴加 KSCN 溶液,若观察到现象:_____,则猜想 b 不成立。
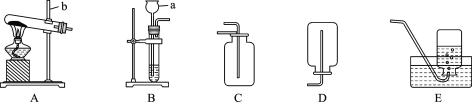
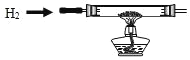
方案二:如图,向该黑色固体通入足量的氢气充分反应。通过称量反应前、后的固体质量,再通过简单计算来分析确定固体的成分。
①在进行方案二时,小杰称得的固体质量如下:
反应前 | 反应后 |
玻璃管的质量为 91 克,固体质量为A 克 | 玻璃管和固体物质的总质量为(91+B)克 |
②有同学认为如图所示装置,加热先通一会儿气体 X 再通入氢气,停止加热后再通一会儿氢气,这样可使实验测得的数据更加准确。你认为在O2、N2 和Ne 三种气体中,气体 X 最没有可能的是__________。
③通过计算后,你认为 A:B 的范围是_________时,猜想 d 成立。
【答案】剧烈燃烧,火星四射,放出大量热(答到火星四射即给分) Fe3O4+4H2SO4=Fe2(SO4)3+FeSO4+4H2O 氧化铁不是黑色的(或氧化铁是红色的) FeO(或氧化亚铁) Fe2+ Fe2(SO4)3 FeSO4 H2SO4(写全才得分) 溶液变为血红色 O2(或氧气) 9:7至29:21(不化简或者数据倒过来都给分)
【解析】
(1)铁丝在氧气中燃烧,除了生成黑色固体外还观察到铁丝剧烈燃烧,火星四射,放出大量热。
[查阅资料]
①Fe3O4 和稀硫酸反应生成铁盐、亚铁盐和水 ,该反应的化学方程式为 ![]() 。
。
[猜 想]
猜想a. 该黑色固体不是Fe2O3, 因为氧化铁是红色的。
猜想b. 该黑色固体是氧化亚铁,因为氧化亚铁是黑色的。
[实验设想]
如果猜想 b 成立,黑色固体是氧化亚铁,氧化亚铁与稀硫酸反应生成硫酸亚铁和水,则反应后溶液中所含的金属离子是亚铁离子,符号为Fe2+。
如果猜想c 成立,该黑色固体是Fe3O4,四氧化三铁与稀硫酸反应生成硫酸铁、硫酸亚铁和水,则反应后溶液中所含的溶质有生成的![]() 和FeSO4,以及过量的H2SO4。
和FeSO4,以及过量的H2SO4。
[实验方案]
方案一:取上述固体于烧杯中,加入适量的稀硫酸,过滤后向滤液中滴加 KSCN 溶液,猜想 b 不成立,则溶液中含有铁离子,铁离子遇到KSCN溶液变为血红色。
方案二:②加热前先通一会儿气体 X 再通入氢气,目的是把管内的空气排出来,防止加热氢气时发生爆炸,所以,气体 X 最没有可能的是氧气,因为氢气与氧气混合加热可能发生爆炸。
③根据质量守恒定律可知,铁的氧化物与氢气完全反应时,固体减少的质量就是氧化物中氧元素的质量。假设A全部是氧化亚铁时,A与B的质量比为氧化亚铁的质量与氧化亚铁中铁元素的质量之比,则有:![]() ,解得A:B=9:7;假设A全部是四氧化三铁时,A与B的质量比为四氧化三铁的质量与四氧化三铁中铁元素的质量之比,则有:
,解得A:B=9:7;假设A全部是四氧化三铁时,A与B的质量比为四氧化三铁的质量与四氧化三铁中铁元素的质量之比,则有:![]() ,解得A:B=29:21。猜想 d 成立,黑色固体中既有氧化亚铁也有四氧化三铁,则A:B的范围是9:7至29:21。
,解得A:B=29:21。猜想 d 成立,黑色固体中既有氧化亚铁也有四氧化三铁,则A:B的范围是9:7至29:21。