题目内容
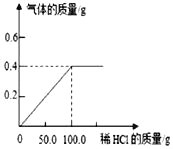
【题目】将一定量的稀盐酸逐渐加入到30g黄铜(铜锌合金)样品中,恰好完全反应,产生气体质量与加入稀盐酸质量的关系如图所示。试计算:
(1)样品中含锌的质量;
(2)所用稀盐酸中溶质的质量分数;
(3)将反应后溶液蒸发44.6g水仍无晶体析出,计算溶液中溶质的质量分数。
【答案】13g、14.6%、40%
【解析】
解:设参加反应的锌的质量为x,所用稀盐酸中溶质的质量分数为y,生成的氯化锌的质量为z,
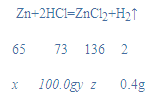
![]() x=13g;
x=13g;
![]() y=14.6%;
y=14.6%;
![]() z=27.2g;
z=27.2g;
将反应后溶液蒸发44.6g水仍无晶体析出,溶液中溶质的质量分数为![]() ×100%=40%;
×100%=40%;
答:(1)样品中含锌的质量为13g;
(2)所用稀盐酸中溶质的质量分数为14.6%;
(3)将反应后溶液蒸发44.6g水仍无晶体析出,溶液中溶质的质量分数为40%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目