题目内容
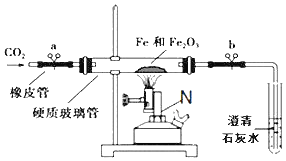
【题目】下图为实验室用一氧化碳还原氧化铁的实验装置图。
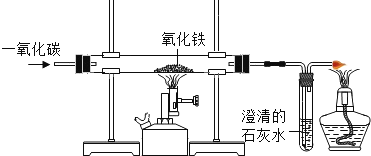
(1)硬质玻璃管中的实验现象是________,该化学反应方程式为_________。
(2)右边试管中的澄清石灰水中产生的实验现象是____,化学反应方程式是_______。
(3)实验过程中,常在装置图的末端的导管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是___。
(4)通过此实验,我们可认识到CO和CO2的化学性质有许多的不同。请写出其中的一点:_______。
(5)试从微观的角度分析CO和CO2化学性质不同的原因:________。
【答案】红色粉末变成黑色 3CO+Fe2O3![]() 2Fe+3CO2 澄清的石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 防止一氧化碳污染空气 一氧化碳可燃,二氧化碳不可燃(合理即可) 分子结构不同
2Fe+3CO2 澄清的石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 防止一氧化碳污染空气 一氧化碳可燃,二氧化碳不可燃(合理即可) 分子结构不同
【解析】
(1)一氧化碳还原氧化铁在加热的条件下生成铁和二氧化碳,红色粉末变成黑色,化学反应方程式为:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(2)二氧化碳能使澄清的石灰水变浑浊,原因是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,化学反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(3)尾气中含有有毒的一氧化碳气体,直接排放会污染空气,一氧化碳能燃烧生成二氧化碳,不会污染空气;
(4)由该实验可知一氧化碳可燃,二氧化碳不可燃,二氧化碳能使澄清的石灰水变浑浊,一氧化碳不能等;
(5)分子是保持物质化学性质的最小粒子,一氧化碳和二氧化碳的分子结构不同,决定了二者的性质不同。

练习册系列答案
相关题目