题目内容
【题目】用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如下图所示(图中横、纵坐标分别表示反应时间t和产生氢气的质量m).试回答:
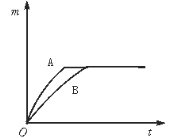
(1)曲线A表示的是_____(填“铁”或“锌”)跟稀硫酸反应的情况.
(2)上述反应中一定没有剩余的物质是_____(填化学式)
(3)上述反应中一定有剩余的金属是_____(填化学式)
【答案】锌 ![]() Fe
Fe
【解析】
用相同质量的铁和锌跟一定量的稀硫酸反应,锌的金属活动性大于铁,锌与稀硫酸反应的速度比铁与稀硫酸反应的速度要快,因此图中曲线A表示的是锌与稀硫酸反应产生氢气的质量时间关系图,曲线B表示的是铁与稀硫酸反应产生氢气的质量时间关系图,锌、铁分别与稀硫酸反应的质量关系为:每65份质量的锌与98份质量的硫酸反应生成2份质量的氢气,每56份质量的铁与98份质量的硫酸反应生成2份质量的氢气,二者最终产生氢气的质量相等,说明两种金属均过量或者锌与稀硫酸恰好完全反应,铁有剩余,没有反应完。根据以上分析有:
(1)曲线A表示的是锌跟稀硫酸反应的情况;
(2)上述反应中一定没有剩余的物质是![]() ;
;
(3)上述反应中一定有剩余的金属是Fe。

练习册系列答案
相关题目