题目内容
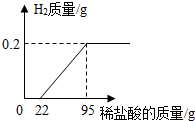 工业上常用稀盐酸除去钢铁表面的铁锈,某小组将一根表面锈蚀的铁钉投入到150g稀盐酸中(假设盐酸将铁锈消耗完后才与铁反应),反应数据如图所示.试求:
工业上常用稀盐酸除去钢铁表面的铁锈,某小组将一根表面锈蚀的铁钉投入到150g稀盐酸中(假设盐酸将铁锈消耗完后才与铁反应),反应数据如图所示.试求:(1)与铁锈反应消耗稀盐酸的质量为
(2)所用稀盐酸溶液的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)盐酸与铁锈反应时无气体生成,故由图可知,与铁锈反应消耗稀盐酸的质量为22g;
(2)由图可知,与铁反应生成0.2g氢气时消耗的盐酸的质量为:95g-22g=73g,根据盐酸与铁反应的化学方程式和氢气的质量求出73g盐酸中氯化氢的质量,进而求质量分数.
(2)由图可知,与铁反应生成0.2g氢气时消耗的盐酸的质量为:95g-22g=73g,根据盐酸与铁反应的化学方程式和氢气的质量求出73g盐酸中氯化氢的质量,进而求质量分数.
解答:解:(1)盐酸与铁锈反应时无气体生成,故由图可知,与铁锈反应消耗稀盐酸的质量为22g;
故答案为:22;
(2)由图可知,与铁反应生成0.2g氢气时消耗的盐酸的质量为:95g-22g=73g,
设73g盐酸中氯化氢的质量为x
Fe+2HCl═FeCl2+H2↑
73 2
x 0.2g
=
x=7.3g
所用稀盐酸溶液的溶质质量分数:
×100%=10%.
答:所用稀盐酸溶液的溶质质量分数为10%.
故答案为:22;
(2)由图可知,与铁反应生成0.2g氢气时消耗的盐酸的质量为:95g-22g=73g,
设73g盐酸中氯化氢的质量为x
Fe+2HCl═FeCl2+H2↑
73 2
x 0.2g
| 73 |
| 2 |
| x |
| 0.2g |
x=7.3g
所用稀盐酸溶液的溶质质量分数:
| 7.3g |
| 73g |
答:所用稀盐酸溶液的溶质质量分数为10%.
点评:根据图示明确反应过程、掌握计算的基本格式是正确解决本题的关键.

练习册系列答案
相关题目
下列燃料中被称为是未来绿色能源的是( )
| A、煤 | B、石油 | C、天然气 | D、氢气 |

 和
和 分别表示两种不同元素的原子,则其中表示混合物的是
分别表示两种不同元素的原子,则其中表示混合物的是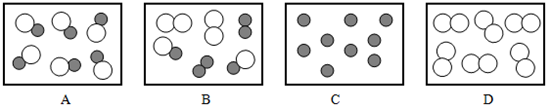
 为测定某盐酸的溶质质量分数,小荣同学取该盐酸样品50g,向其中加入过量锌粒,完全反应后手机到0.3g氢气,请完成下列计算与分析:
为测定某盐酸的溶质质量分数,小荣同学取该盐酸样品50g,向其中加入过量锌粒,完全反应后手机到0.3g氢气,请完成下列计算与分析: 如图是稀释浓硫酸实验的示意图.
如图是稀释浓硫酸实验的示意图.