题目内容
【题目】化学是在分子、原子层次上研究物质的科学:
(1)构成物质的粒子有分子、原子和__________。
(2)下图为三种元素的原子结构示意图。
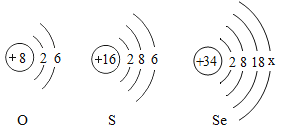
①氧原子在化学反应中容易________电子(填“得到”或“失去”)。
②硒元素能增强人体免疫力,延缓衰老,山药等食物中富含硒元素。硒(Se)在氧气中燃烧生成二氧化硒。回答下列问题:
A图中x的值为_________。
B硒元素与氧、硫元素的化学性质相似,原因是它们的原子_____________相同
C已知硒(Se)元素相对原子质量为79,则硒原子核内的中子数为_____________。
【答案】离子 得到 6 最外层电子数 45
【解析】
(1)构成物质的粒子有分子、原子和离子;
(2)①氧原子的最外层电子数是6,大于4,在化学反应中易得到2个电子而形成带2个单位负电荷的氧离子;
②A、对于原子质子数等于核外电子数,故图中x的值为34-2-8-18=6;
B、元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是最外层电子数,硒元素与氧、硫元素的化学性质相似的原因是它们原子的最外层的电子数相同。
C、硒的质子数是34,相对原子质量![]() 质子数+中子数,则中子数是:79-34=45。
质子数+中子数,则中子数是:79-34=45。

 优学名师名题系列答案
优学名师名题系列答案【题目】下面是小婷同学测定黄铜(铜锌合金)中铜的质量分数的过程。小婷同学取10 g黄铜于烧杯中,将120 g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
次数 | 一 | 二 | 三 | 四 | 五 | 六 |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 29.96 | 49.92 | m | 89.84 | 109.8 | 129.8 |
①10g黄铜完全反应产生H2的质量________g;
②表中m=________;
③求黄铜中铜的质量分数________ (写出计算过程)。
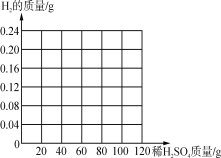
④请在如图画出10g黄铜加入稀硫酸与生成氢气的质量的图象________。
【题目】兴趣小组同学在探究金属的化学性质和金属锈蚀的条件时,分别做了如下两个探究实验,请你一起参与,并完成相关问题。
探究一:探究金凤的活动性顺序。
将锌、铁、铜三种金属分别放人稀硫酸、硫酸铜溶液、硝酸银溶液、氯化钠溶液中,观察并记录现象如下表:
金属 | 稀硫酸 | 硫酸铜溶液 | 硝酸银溶液 | 氯化钠溶液 |
锌 | √①剧烈 | √ | √ | 一 |
铁 | √不剧烈 | √② | √ | 一 |
铜 | 一 | 一 | √③ | 一 |
注明:用“√”表示能观察到实验现象,用“一”表示观察不到实验现象。
(1)分别写出①、②中观察到的实验现象________;
(2)③中发生反应的化学方程式为_________;
(3)运用“控制变量法”设计实验方案是化学研究的重要方法。在锌、铁、铜与稀硫酸实验中,需要控制的实验条件除了金属与稀硫酸接触面积稀硫酸的体积、温度以外,还需要控制的条件是_____;
(4)上述实验涉及到的五种金属的活动性由强到弱的顺序是______(用元素符号表示);
(5)若利用上述试剂制取氢气,小明认为应该选择金属锌和稀硫酸反应,而不选择金属铁和稀硫酸反应,其理由是_______;
探究二:探究金属锈蚀的条件。
[实验步骤]在下列五只试管中分别放人完全相同的洁净铁钉,几天后观察铁钉锈蚀的情况。
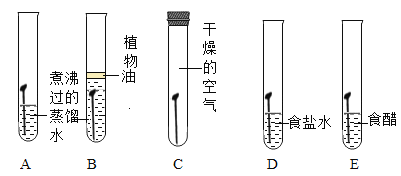
[现象记录]A、D、E中铁钉锈蚀明显,B、C中铁钉不生锈。
[结论与解释](1)对比A、B实验.说明铁锈蚀一定要有_______参加;对比A、C实验,说明铁生锈要有______参加;
(2)试管D和E的实验目的是探究铁在________或_______存在的环境中更易锈蚀;
(3)写出一种防止铁制品生锈的具体方法_______;