题目内容
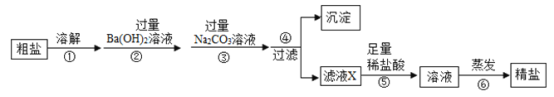
【题目】粗盐的主要成分是NaCl,下面是除去粗盐中MgCl2、Na2SO4、CaCl2等杂质的流程图(提示:微溶物不形成沉淀)
(1)写出操作②中发生的化学反应方程式(写出一个即可)
_______________。
(2)写出加入过量Na2CO3溶液的目的。
_______________。
(3)滤波X中含有几种溶质?
_______________。
【答案】![]() 或
或![]() 除氯化钙、氯化钡和过量的氢氧化钡(除去Ca2+、Ba2+) 三种溶质(氯化钠、碳酸钠和氢氧化钠;或NaCl、Na2CO3、NaOH)
除氯化钙、氯化钡和过量的氢氧化钡(除去Ca2+、Ba2+) 三种溶质(氯化钠、碳酸钠和氢氧化钠;或NaCl、Na2CO3、NaOH)
【解析】
①溶解过滤先除去不溶性杂质;
②加入过量的氢氧化钡溶液,可以同时除去杂质氯化镁、硫酸钠,生成的氢氧化钠、氯化钡和过量的氢氧化钡是新的杂质;
③加入的过量碳酸钠可以除去杂质氯化钙、氯化钡和氢氧化钡,过滤后,滤液X中含有氯化钠、氢氧化钠和碳酸钠;
④过滤将生成的沉淀与溶液分离;
⑤足量稀盐酸除去溶液中的Na2CO3、NaOH,使溶液中只有氯化钠,和过量的盐酸;
⑥蒸发的过程中,先将盐酸的溶质氯化氢挥发除去,再继续蒸发使水蒸发,得到精盐。
(1)根据分析可知,步骤②中涉及到的反应有为:氢氧化钡和氯化镁反应生成氢氧化镁沉淀和氯化钡。或氢氧化钡和硫酸镁反应生成硫酸钡沉淀和氢氧化钠。故答案为:![]() 或
或![]() ;
;
(2)通过分析可知,加入过量的Na2CO3的目的是除去氯化钙、氯化钡、过量的氢氧化钡。故答案为:除氯化钙和氯化钡、过量的氢氧化钡(或回答:除去Ca2+、Ba2+);
(3)通过分析可知,滤液X中的溶质有三种,分别是氯化钠、碳酸钠、氢氧化钠。故答案为:三种溶质(或回答:氯化钠、碳酸钠和氢氧化钠;或回答:NaCl、Na2CO3、NaOH)。

练习册系列答案
相关题目