题目内容
(1)计算甲烷(CH4)中碳、氢两元素的质量比
(2)用化学方程式计算:
在二氧化锰做催化剂的条件下完全分解3.4克过氧化氢,可生成氧气的质量为多少克?
(2)用化学方程式计算:
在二氧化锰做催化剂的条件下完全分解3.4克过氧化氢,可生成氧气的质量为多少克?
考点:元素质量比的计算,根据化学反应方程式的计算
专题:化学式的计算,有关化学方程式的计算
分析:(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)由完全分解过氧化氢的质量为3.4克,由反应的化学方程式计算出生成氧气的质量即可.
(2)由完全分解过氧化氢的质量为3.4克,由反应的化学方程式计算出生成氧气的质量即可.
解答:解:(1)甲烷(CH4)中碳、氢两元素的质量比为12:(1×4)=3:1.
(2)设可生成氧气的质量为x
2H2O2
2H2O+O2↑
68 32
3.4g x
=
x=1.6g
答:(1)3:1;(2)可生成氧气的质量为1.6g.
(2)设可生成氧气的质量为x
2H2O2
| ||
68 32
3.4g x
| 68 |
| 32 |
| 3.4g |
| x |
答:(1)3:1;(2)可生成氧气的质量为1.6g.
点评:本题难度不大,掌握化学式的有关计算、化学方程式的计算是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
日常生活中,区别下列各组物质所用的方法,错误的是( )
| A、白酒和白醋--观察颜色 |
| B、食盐和面碱--加醋,看气泡 |
| C、黄铜和黄金--灼烧,观察颜色变化 |
| D、聚乙烯塑料和聚氯乙烯塑料--灼烧,闻气味 |
 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: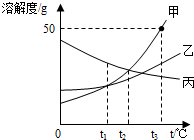 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空: