题目内容
已知水垢中一定含CaCO3,可能含MgCO3、Mg(OH)2等。取5.78g不含结晶水的水垢样品灼烧后,将产生的气体全部通入足量的澄清石灰水中得到CaCO3 6.00 g。则下列说法正确的是
- A.该样品一定不含有MgCO3
- B.该样品一定含MgCO3
- C.该样品灼烧后的固体产物中仅有CaO
- D.该样品灼烧后固体产物有CaO、MgO
试题分析:本题涉及的化学反应方程式为
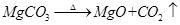 ,
, ,由方程式可知,碳酸镁和碳酸钙的个数比为1:1,所以它们的质量比为84:100,所以产生6g碳酸钙一定会对应有5.04g碳酸镁,剩余的5.78g-5.04g=0.74g物质为氢氧化镁,所以该样品灼烧后固体产物有CaO、MgO。
,由方程式可知,碳酸镁和碳酸钙的个数比为1:1,所以它们的质量比为84:100,所以产生6g碳酸钙一定会对应有5.04g碳酸镁,剩余的5.78g-5.04g=0.74g物质为氢氧化镁,所以该样品灼烧后固体产物有CaO、MgO。考点:常见化学反应的推断
点评:利用化学反应判断物质组成的题目属于中考常考的知识点,通常在探究题中出现,考察基础知识和化学实验思想,注意仔细审题。

某校化学小组对热水壶底部水垢的主要成分进行了'如下探究,请完成以下活动并回答相关问题。
【查阅资料】
天然水中含有![]() 、
、![]() 、
、![]() 等离子,在加热条件下,这些离子趋于生成溶解度更小的物质――水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表:
等离子,在加热条件下,这些离子趋于生成溶解度更小的物质――水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表:
部分钙、镁化合物溶解性表(20℃)
| 阴离子 阳离子 |
|
|
|
|
| 微溶 | 不溶 | 可溶 |
|
| 不溶 | 微溶 | 可溶 |
【提出猜想】
水垢的主要成分中一定含有 和 ,可能含有Ca(OH)2和MgCO3(填化学式)。
【设计方案】
实验1:确定水垢中是否含Ca(OH)2和CaCO3。
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液 | 没有白色沉淀产生 | _________________________ |
实验2:确定水垢是否含MgCO3。
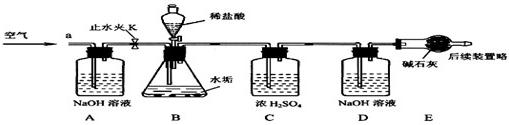
利用下列实验装置,完成实验2探究。其主要实验步骤如下:

称量D、E装置总质量为600.00g,按上图组装后,将2.50g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为601.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响)。
【实验讨论】
(1)加入样品前还应 ,装置B中盛放稀盐酸的仪器名称为 ,装置C的作用是 ,反应结束后打开止水夹K,缓缓鼓入空气的目的是 ,装置A的作用是 。A、B装置之间 设置干燥装置(填“要”、“不要”),其理由是 。
(2)装置B中生成气体的化学反应方程式为 (只要求写一种),装置D中的化学反应方程式为 。
(3)装置B中生成CO2的质量为 g。通过计算说明水垢中 含MgCO3(填字母)。
A.一定 B.一定不 C.可能 D.无法确定
计算过程(已知物质相对分子质量CaCO3:100,MgCO3:84):
实验3:确定水垢中是否含有Mg(OH)2。
另取质量为2.50g水垢,加3.65%稀盐酸与之反应,测得消耗稀盐酸![]() g。结合以上实验结论,判断当
g。结合以上实验结论,判断当![]() 的值满足 条件时,水垢中一定含有Mg(OH)2(请通过计算说明)。
的值满足 条件时,水垢中一定含有Mg(OH)2(请通过计算说明)。
[查阅资料]天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见表
| 部分钙、镁化合物溶解性表(20℃) | |||
| 阴离子阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
[设计方案]实验1:确定水垢中是否含Ca(OH)2和CaCO3
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入 Na2CO3溶液. | 没有白色沉淀产生 | ______ |
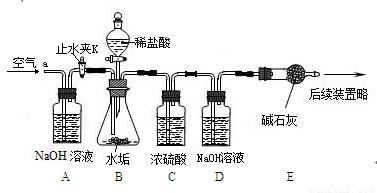
称量D、E装置总质量为600.00g,按上图组装后,将2.50g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为601.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响).
[实验讨论](1)加入样品前还应______,装置B中盛放稀盐酸的仪器名称为______,装置C的作用是______,反应结束后打开止水夹K,缓缓鼓入空气的目的是______,装置A的作用是______,A、B装置之间设置干燥装置(填:“要”、“不要”),______理由是______.
(2)装置B中生成气体的化学方程式为______(只要求写一种),装置D中的化学方程式为______.
(3)装置B中生成CO2的质量为______g.通过计算说明水垢中______含MgCO3(填字母).
A. 一定B. 一定不C. 可能D. 无法确定
计算过程(已知物质相对分子质量 CaCO3:100 MgCO3:84):
实验3:确定水垢中是否含有Mg(OH)2另取质量为2.50g的水垢,加入3.65%的稀盐酸与之反应,测得消耗稀盐酸w g..结合以上实验结论,判断w的值满足______条件时,水垢中一定含有Mg(OH)2(请通过计算说明).
[查阅资料]天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见表
| 部分钙、镁化合物溶解性表(20℃) | |||
| 阴离子阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
[设计方案]实验1:确定水垢中是否含Ca(OH)2和CaCO3
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入 Na2CO3溶液. | 没有白色沉淀产生 | ______ |

称量D、E装置总质量为600.00g,按上图组装后,将2.50g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为601.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响).
[实验讨论](1)加入样品前还应______,装置B中盛放稀盐酸的仪器名称为______,装置C的作用是______,反应结束后打开止水夹K,缓缓鼓入空气的目的是______,装置A的作用是______,A、B装置之间设置干燥装置(填:“要”、“不要”),______理由是______.
(2)装置B中生成气体的化学方程式为______(只要求写一种),装置D中的化学方程式为______.
(3)装置B中生成CO2的质量为______g.通过计算说明水垢中______含MgCO3(填字母).
A. 一定B. 一定不C. 可能D. 无法确定
计算过程(已知物质相对分子质量 CaCO3:100 MgCO3:84):
实验3:确定水垢中是否含有Mg(OH)2另取质量为2.50g的水垢,加入3.65%的稀盐酸与之反应,测得消耗稀盐酸w g..结合以上实验结论,判断w的值满足______条件时,水垢中一定含有Mg(OH)2(请通过计算说明).
[查阅资料]天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见表
| 部分钙、镁化合物溶解性表(20℃) | |||
| 阴离子阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
[设计方案]实验1:确定水垢中是否含Ca(OH)2和CaCO3
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入 Na2CO3溶液. | 没有白色沉淀产生 | ______ |
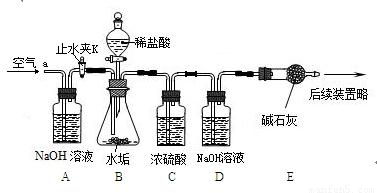
称量D、E装置总质量为600.00g,按上图组装后,将2.50g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为601.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响).
[实验讨论](1)加入样品前还应______,装置B中盛放稀盐酸的仪器名称为______,装置C的作用是______,反应结束后打开止水夹K,缓缓鼓入空气的目的是______,装置A的作用是______,A、B装置之间设置干燥装置(填:“要”、“不要”),______理由是______.
(2)装置B中生成气体的化学方程式为______(只要求写一种),装置D中的化学方程式为______.
(3)装置B中生成CO2的质量为______g.通过计算说明水垢中______含MgCO3(填字母).
A. 一定B. 一定不C. 可能D. 无法确定
计算过程(已知物质相对分子质量 CaCO3:100 MgCO3:84):
实验3:确定水垢中是否含有Mg(OH)2另取质量为2.50g的水垢,加入3.65%的稀盐酸与之反应,测得消耗稀盐酸w g..结合以上实验结论,判断w的值满足______条件时,水垢中一定含有Mg(OH)2(请通过计算说明).